题目内容
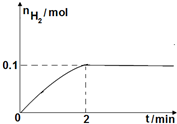
8.在密闭的容器中进行如下反应:X(g)+2Y(g)?3Z(g),根据图象对应的叙述一定正确的是( )
| A. | a与b比较,b使用了催化剂 | B. | a与b比较,b温度更高 | ||
| C. | a与b比较,b的压强更大 | D. | a与b比较,b反应速率更大 |
分析 化学反应X(g)+2Y(g)?3Z(g),是气体体积不变的反应,压强改变对化学平衡无影响,图象分析可知反应a和b达到平衡状态X的转化率相同,只是达到平衡状态所需时间不同,说明可能是催化剂对反应速率的影响,或是增大压强对反应速率的影响;
解答 解:X(g)+2Y(g)?3Z(g),是气体体积不变的反应,压强改变对化学平衡无影响,a和b达到平衡状态X的转化率相同,说明是相同的平衡状态,只是达到平衡状态所需时间不同,说明可能是催化剂对反应速率的影响,或是增大压强对反应速率的影响,催化剂只改变化学反应速率,缩短达到平衡的时间,不改变化学平衡,
A.a与b比较,b可能使用了催化剂或增大反应体系的压强,故A错误;
B.化学反应过程中一定伴随着能量的变化,温度改变化学平衡一定发生移动,X的转化率一定发生变化,不符合图象变化,故B错误;
C.a与b比较,b可能使用了催化剂或增大反应体系的压强,不一定是压强增大,故C错误;
D.a与b比较,达到相同平衡状态,b所需时间短,说明反应速率快,所以b反应速率更大,故D正确;
故选D.
点评 本题考查了影响化学平衡,化学反应速率的因素分析判断,图象的变化特征理解应用,注意达到相同平衡状态的建立过程分析,题目难度中等.

练习册系列答案
相关题目
9.0.5mol 气态烃A 最多和1mol HCl加成,生成氯代烷B,1mol B与4mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )
| A. | C2H4 | B. | C2H2 | C. | C3H4 | D. | C4H6 |
7.下列叙述正确的是( )
| A. | 含有6.02×1023个氦原子的氦气在标准状况下的体积约为11.2 L | |
| B. | 在常温常压下,11.2 L Cl2含有的分子数为0.5×6.02×1023 | |
| C. | 25℃,1.01×105Pa,64 g SO2中含有的原子数为3×6.02×1023 | |
| D. | 标准状况下,11.2 L H2O含有的分子数为0.5×6.02×1023 |
18.下列离子方程式书写正确的是( )
| A. | 向50 mL 1 mol•L-1明矾溶液中滴入少量0.1 mol•L-1Ba(OH)2溶液Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| B. | 已知还原性Fe2+>Br-,a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4C1- | |
| C. | 向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I-═3I2+2H2O | |
| D. | 在澄清石灰水中加入适量碳酸氢镁溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
 硫一碘循环分解水制氢主要涉及下列反应:
硫一碘循环分解水制氢主要涉及下列反应: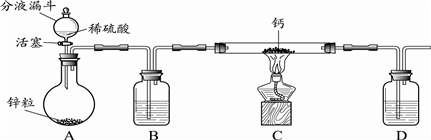
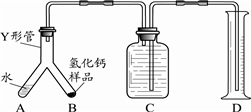
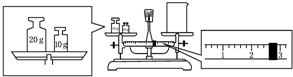 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液245mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液245mL: