题目内容
17. 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液245mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液245mL:(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④转移 ⑤倒转摇匀 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为②①③⑧④⑥⑦⑤.本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯,还有胶头滴管,250 mL容量瓶.
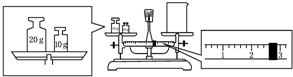
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为27.4 g,要完成本实验该同学应称出10.0 g NaOH.
(3)使用容量瓶前必须进行的一步操作是检漏.
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏低的是③④⑥.
①定容时俯视刻度线
②容量瓶不干燥,含有少量蒸馏水
③没有洗涤烧杯和玻璃棒
④转移溶液时不慎有少量洒到容量瓶外面
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
分析 (1)配制溶液的一般步骤步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,据此排序,确定需要的仪器和缺少的仪器;
(2)根据左码右物称量药品时,药品的实际质量=砝码的质量-游码的质量;依据m=CVM计算需要的溶质的质量;
(3)容量瓶带有瓶塞,使用前应检查是否漏水;
(4)分析操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解:(1)配制溶液的一般步骤步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,所以正确的步骤:②①③⑧④⑥⑦⑤;用到的仪器:天平、药匙、玻璃棒、烧杯、胶头滴管、250 mL容量瓶,还缺少的仪器:胶头滴管、250 mL容量瓶;
故答案为:②①③⑧④⑥⑦⑤; 胶头滴管; 250 mL容量瓶
(2)图中物质和砝码的位置放反了,质量关系应为:砝码的质量=烧杯的质量+游码显示的质量.即30 g=烧杯的质量+2.6 g,得烧杯的质量为:30g-2.6g=27.4g;1.0mol•L-1的NaOH溶液245mL,应选择250mL容量瓶,需要溶质的质量m=1.0mol/L×40g/mol×0.25L=10.0g;
故答案为:27.4;10.0;
(3)容量瓶带有瓶塞,使用前应检查是否漏水;
故答案为:检漏;
(4)①定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故不选;
②容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量和溶液的体积都不会产生影响,溶液浓度不受影响,故不选;
③没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故选;
④转移溶液时不慎有少量洒到容量瓶外面,导致溶质的物质的量偏小,溶液浓度偏低,故选;
⑤未冷却到室温就将溶液转移到容量瓶并定容,冷却后,溶液的体积偏小,溶液浓度偏高,故不选;
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏小,故选;
故选:③④⑥.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和配制步骤是解题关键,注意容量瓶规格的选择和误差分析方法,注意托盘天平使用方法及注意事项,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 溶液褪色 | B. | 产生白色沉淀 | C. | 无明显现象 | D. | 产生黄色沉淀 |

| A. | a与b比较,b使用了催化剂 | B. | a与b比较,b温度更高 | ||
| C. | a与b比较,b的压强更大 | D. | a与b比较,b反应速率更大 |
| A. | 某溶液与NaOH溶液共热.产生能使湿润的红色石蕊试纸变蓝的气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入盐酸后有无色气体产生,该气体能够使澄清的石灰水变浑浊,则原溶液中含CO32- | |
| C. | 用铂丝蘸取某溶液在酒精灯的火焰上灼烧时.火焰呈黄色,说明原溶液中只含有Na+,不含有K+ | |
| D. | 某溶液中加入BaCl2溶液时,产生白色沉淀,加稀硝酸沉淀不溶解,说明原溶液中存在SO42- |
| 金属 | Na | Cu | Al | Fe |
| 熔点/℃ | 97.5 | 1 083 | 660 | 1 535 |
| 沸点/℃ | 883 | 2 595 | 2 200 | 3 000 |
| A. | Cu与Na | B. | Fe与Cu | C. | Fe与Al | D. | Al与Na |
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与硝酸反应:Fe3O4+8H+ ═Fe2++2Fe3++4H2O | 书写正确 |
| B | 工业制粗硅:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | 错误,生成物应是Si和CO |
| C | NaAlO2溶液与少量CO2反应: AlO2- ̄+CO2+2H2O═HCO3- ̄+Al(OH)3↓ | 书写正确 |
| D | NaHCO3溶液中加入少量石灰水:Ca2++2OH-+2HCO-3=CaCO3↓+CO32-+2H2O | 错误,生成物 中不含CO32- |
| A. | A | B. | B | C. | C | D. | D |
| A. | C消耗的速率与A消耗的速率相等 | |
| B. | 单位时间内生成a mol B,同时消耗a mol C | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体的密度不再变化 |
