题目内容
下列各表述与示意图一致的是( )
A、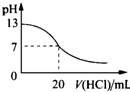 此图表示25℃时,用0.1mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 |
B、 此图表示一定条件下进行的反应2SO2(g)+O2(g)═2SO3(g)△H<0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 |
C、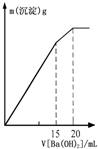 此图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
D、 此图表示化学反应H2(g)+C12(g)═2HCl(g)的能量变化,则该反应的反应热△H=﹢183kJ/mol |
考点:酸碱混合时的定性判断及有关ph的计算,离子方程式的有关计算,反应热和焓变,物质的量或浓度随时间的变化曲线
专题:图示题
分析:A、等浓度、等体积的氢氧化钠与盐酸反应,在滴定终点时pH会发生突变;
B、根据图象可知,t2时刻反应物物质的量减小,生成物浓度增加,说明平衡向着正向移动,根据影响化学平衡的因素分析;
C、铝离子恰好完全沉淀时,沉淀的总质量没有达到最大,即在加入氢氧化钡溶液15mL处;
D、根据反应物、生成物总能量可以判断出该反应为放热反应,焓变应该小于0.
B、根据图象可知,t2时刻反应物物质的量减小,生成物浓度增加,说明平衡向着正向移动,根据影响化学平衡的因素分析;
C、铝离子恰好完全沉淀时,沉淀的总质量没有达到最大,即在加入氢氧化钡溶液15mL处;
D、根据反应物、生成物总能量可以判断出该反应为放热反应,焓变应该小于0.
解答:
解:A、0.1mol?L-1NaOH溶液的pH为13,用0.1mol?L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错误;
B、因反应为体积减小的放热反应,则降低温度或增大压强,平衡向着正向移动,二氧化硫、氧气的物质的量减小,三氧化硫的物质的量增大,图象与反应情况一致,故B正确;
C、当Al3+完全沉淀时,离子方程式为2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓;当SO42-完全沉淀时,离子方程式为Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,可见加入15mL氢氧化钡溶液时,铝离子完全沉淀,最后氢氧化铝沉淀逐渐溶解,硫酸钡沉淀逐渐增加,沉淀的质量继续增大,当硫酸根离子完全转化成硫酸钡沉淀时,氢氧化铝完全溶解,即加入20mL氢氧化钡溶液时代表SO42-完全沉淀,铝离子完全溶解,故C错误;
D、分析图象拆化学键和形成化学键能量变化判断,该反应是放热反应,反应热△H=-183kJ/mol,故D错误;
故选B.
B、因反应为体积减小的放热反应,则降低温度或增大压强,平衡向着正向移动,二氧化硫、氧气的物质的量减小,三氧化硫的物质的量增大,图象与反应情况一致,故B正确;
C、当Al3+完全沉淀时,离子方程式为2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓;当SO42-完全沉淀时,离子方程式为Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,可见加入15mL氢氧化钡溶液时,铝离子完全沉淀,最后氢氧化铝沉淀逐渐溶解,硫酸钡沉淀逐渐增加,沉淀的质量继续增大,当硫酸根离子完全转化成硫酸钡沉淀时,氢氧化铝完全溶解,即加入20mL氢氧化钡溶液时代表SO42-完全沉淀,铝离子完全溶解,故C错误;
D、分析图象拆化学键和形成化学键能量变化判断,该反应是放热反应,反应热△H=-183kJ/mol,故D错误;
故选B.
点评:本题考查了酸碱中和滴定曲线判断、反应热和焓变、离子方程式的有关计算等知识,题目难度中等,注意掌握根据图象判断反应热与焓变的方法,明确外界条件对化学平衡的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、在常温常压下,1.7g NH3含有的原子数为0.4NA |
| C、标准状况下,11.2L水中含有的原子数是1.5NA |
| D、0.2mol?L-1的Na2SO4溶液中含Na+数目为0.4NA |
常温下,在
=1×1012的溶液中,下列各组离子能大量共存的是( )
| c(H+) |
| c(OH-) |
| A、Fe2+、Mg2+、NO3-、SO42- |
| B、Fe3+、Na+、Cl-、SCN- |
| C、NH4+、Al3+、NO3-、Cl- |
| D、Ca2+、K+、Cl-、HCO3- |
有关如图装置中的叙述正确的是( )


| A、这是电解NaOH溶液的装置 |
| B、这是一个原电池装置 |
| C、Pt为负极,其电极反应为:O2+2H2O+4e-═4OH- |
| D、Fe为阳极,其电极反应为:Fe-2e-+2OH-═2Fe(OH)2 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L H2O所含的分子数为NA |
| B、铁与足量氯气反应,1mol Fe失去电子数为3NA |
| C、1mol NH4+所含质子数为10NA |
| D、1 mol?L-1CaCl2溶液中所含Ca2+离子的数目为NA |
阿伏加德罗常数为NA,下列说法中正确的是( )
| A、足量Zn与一定量的浓硫酸反应,产生22.4L气体时,转移的电子数一定为2NA |
| B、14g分子式为CnH2n的烯烃中含有的C=C的数目,一定为NA/n |
| C、71g氯气通入足量水中,反应中转移的电子总数为NA |
| D、7.5gSiO2晶体中含有的硅氧键数为0.5NA |
关于pH相同的醋酸和盐酸,下列叙述正确的是( )
| A、取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n |
| B、取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸 |
| C、取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多 |
| D、两种酸中c(CH3COO-)>c(Cl-) |
