题目内容
常温下,在
=1×1012的溶液中,下列各组离子能大量共存的是( )
| c(H+) |
| c(OH-) |
| A、Fe2+、Mg2+、NO3-、SO42- |
| B、Fe3+、Na+、Cl-、SCN- |
| C、NH4+、Al3+、NO3-、Cl- |
| D、Ca2+、K+、Cl-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:
=1×1012的溶液呈酸性,如在酸性条件下,离子之间不发生任何反应,则可大量共存,反之不能,结合离子的性质解答该题.
| c(H+) |
| c(OH-) |
解答:
解:
=1×1012的溶液呈酸性,
A.酸性条件下Fe2+与NO3-发生氧化还原反应而不能大量共存,故A错误;
B.Fe3+与SCN-发生络合反应而不能大量共存,故B错误;
C.酸性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.酸性条件下,HCO3-不能大量共存,故D错误.
故选C.
| c(H+) |
| c(OH-) |
A.酸性条件下Fe2+与NO3-发生氧化还原反应而不能大量共存,故A错误;
B.Fe3+与SCN-发生络合反应而不能大量共存,故B错误;
C.酸性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.酸性条件下,HCO3-不能大量共存,故D错误.
故选C.
点评:本题考查离子共存,为高考常见题型和高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意常见离子的性质和反应类型的判断,难度不大,本题注意B项发生络合反应的特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在密闭容器中,使2mol N2和6mol H2混合发生反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应)下列说法错误的是( )
| A、升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大 |
| B、升高平衡体系的温度(保持体积不变),混合气体的密度不变 |
| C、当反应达到平衡时,N2和H2的浓度比是1:3 |
| D、当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动 |
下列方程式属于水解反应方程式的是( )
| A、H2CO3?HCO3-+H+ |
| B、HCO3-+H2O?H3O++CO32- |
| C、HCO3-+OH-═H2O+CO32- |
| D、CO32-+H2O?HCO3-+OH- |
下列离子方程式书写正确的是( )
| A、Cl2与H2O反应:Cl2+H2O=2H++Cl-+ClO- |
| B、铁和足量稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| C、Al2(SO4)3溶液与氨水反应:Al3++3OH-=Al(OH)3↓ |
| D、Na与H2O反应:2Na+2H2O=2Na++2OH-+H2↑ |
下列各表述与示意图一致的是( )
A、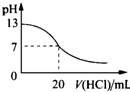 此图表示25℃时,用0.1mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 |
B、 此图表示一定条件下进行的反应2SO2(g)+O2(g)═2SO3(g)△H<0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 |
C、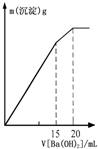 此图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
D、 此图表示化学反应H2(g)+C12(g)═2HCl(g)的能量变化,则该反应的反应热△H=﹢183kJ/mol |
皮肤上若沾上少量的苯酚,正确的处理方法是( )
| A、冷水冲洗 |
| B、用70℃以上热水冲洗 |
| C、用酒精擦洗 |
| D、用稀NaOH溶液清洗 |

