��Ŀ����
������������ʱ��Ҫ�������ݳɷ���ȫ��ͬ��ijӪ��Һ��1L���䷽����������Ƶ���Һ�У�K+�����ʵ���Ũ��Ϊ ��
�䷽����ÿ����Һ�������ʵ�����
ʵ��Ա�������һ����Һʱ���֣�ʵ���ҵ�ZnSO4�Ѿ������ˣ�п����ֻʣ��������п��Zn��NO3��2�����Ȼ�п��ZnCl2������Ϊʵ��Ա������ζ�����õڶ���Ӫ��Һ�����������ʵ����ʵ����������к����У�������Ҫij���ʣ����ڶ�Ӧ���������ϡ�0������
KCl ��K2SO4 ��Zn��NO3��2 ��ZnCl2 ��
�䷽����ÿ����Һ�������ʵ�����
| �Ȼ��� | ����� | ����п |
| 0.3mol | 0.2mol | 0.1mol |
KCl
���㣺���ʵ���Ũ��,Ħ������
ר�⣺������
����������Ӫ��Һ�к��е����ӿ�֪��Ӧ���Ȼ�п��������п��Ӫ��Һ����Ӧ�������ʵ�����ԭӪ��Һ��ȣ��ݴ˼�������䷽���Ȼ��ء�����ء��Ȼ�п�����ʵ�����
���
�⣺ԭ�䷽Ӫ��Һ�У�n��K+��=n��KCl��+2n��K2SO4��=0.3mol+2��0.2mol=0.7mol����Һ���Ϊ1L��c��K+��=0.7mol/L��
n��SO42-��=n��K2SO4��+n��ZnSO4��=0.2mol+0.1mol=0.3mol��
n��Zn2+��=n��ZnSO4��=0.1mol��
n��Cl-��=n��KCl��=0.3mol��
�����䷽��ѡ���Ȼ�п��������п��Ӫ��Һ����Ӧ�������ʵ�����ȣ���
����������n��ZnCl2��=n��Zn2+��=0.1mol��
�������������n��KCl��=n��Cl-��-2n��ZnCl2��=0.3mol-2��0.1mol=0.1mol��
����������������n��K2SO4��=n��SO42-��=0.3mol��
��Һ��n��K+��=n��KCl��+2n��K2SO4��=0.1mol+2��0.7mol=0.7mol��
�ʵ����䷽���£�ѡ���Ȼ�п��������п�����Ҹ��ɷݵ������ֱ�Ϊ���Ȼ��أ�0.1mol������أ�0.3 mol���Ȼ�п��0.1 mol��
���Ȼ�п��������п�����Ҹ��ɷݵ������ֱ�Ϊ���Ȼ��أ�0.1mol������أ�0.3 mol���Ȼ�п��0.1 mol��
�ʴ�Ϊ��0.7mol/L��0.1mol��0.3mol��0��0.1mol��
n��SO42-��=n��K2SO4��+n��ZnSO4��=0.2mol+0.1mol=0.3mol��
n��Zn2+��=n��ZnSO4��=0.1mol��
n��Cl-��=n��KCl��=0.3mol��
�����䷽��ѡ���Ȼ�п��������п��Ӫ��Һ����Ӧ�������ʵ�����ȣ���
����������n��ZnCl2��=n��Zn2+��=0.1mol��
�������������n��KCl��=n��Cl-��-2n��ZnCl2��=0.3mol-2��0.1mol=0.1mol��
����������������n��K2SO4��=n��SO42-��=0.3mol��
��Һ��n��K+��=n��KCl��+2n��K2SO4��=0.1mol+2��0.7mol=0.7mol��
�ʵ����䷽���£�ѡ���Ȼ�п��������п�����Ҹ��ɷݵ������ֱ�Ϊ���Ȼ��أ�0.1mol������أ�0.3 mol���Ȼ�п��0.1 mol��
���Ȼ�п��������п�����Ҹ��ɷݵ������ֱ�Ϊ���Ȼ��أ�0.1mol������أ�0.3 mol���Ȼ�п��0.1 mol��
�ʴ�Ϊ��0.7mol/L��0.1mol��0.3mol��0��0.1mol��
������������Ӫ��Һ����Ϊ���壬������Һ���������ʵ����йؼ��㣬�ѶȲ���ע��������Һ�е���غ㣮

��ϰ��ϵ�д�
�����Ŀ
���и�������ʾ��ͼһ�µ��ǣ�������
A��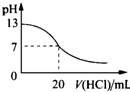 ��ͼ��ʾ25��ʱ����0.1mol/L����ζ�20mL 0.1mol/L NaOH��Һ����Һ��pH�����������ı仯�õ��ĵζ����� |
B�� ��ͼ��ʾһ�������½��еķ�Ӧ2SO2��g��+O2��g���T2SO3��g����H��0���ɷֵ����ʵ����仯��t2ʱ�̸ı�����������ǽ����¶Ȼ���С������� |
C��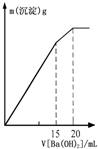 ��ͼ��ʾij������Һ�м���Ba��OH��2��Һ�����������������Ba��OH��2��Һ����Ĺ�ϵ���ڼ���20mL Ba��OH��2��Һʱ������ǡ�ó�����ȫ |
D�� ��ͼ��ʾ��ѧ��ӦH2��g��+C12��g���T2HCl��g���������仯����÷�Ӧ�ķ�Ӧ�ȡ�H=��183kJ/mol |
