题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L H2O所含的分子数为NA |
| B、铁与足量氯气反应,1mol Fe失去电子数为3NA |
| C、1mol NH4+所含质子数为10NA |
| D、1 mol?L-1CaCl2溶液中所含Ca2+离子的数目为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标准状况水不是气体;
B、铁和氯气反应生成氯化铁;
C、依据铵根离子结构计算质子数;
D、溶液体积不知,不能计算钙离子数;
B、铁和氯气反应生成氯化铁;
C、依据铵根离子结构计算质子数;
D、溶液体积不知,不能计算钙离子数;
解答:
解:A、标准状况下,22.4L H2O物质的量不是1mol,所含的分子数不是NA,故A错误;
B、铁与足量氯气反应生成氯化铁,1mol Fe失去电子数为3NA,故B正确;
C、依据氮原子质子数为7,氢原子质子数为1计算,1mol NH4+所含质子数为11NA,故C错误;
D、1 mol?L-1CaCl2溶液中,溶液体积不知,不能计算所含Ca2+离子的数目,故D错误;
故选B.
B、铁与足量氯气反应生成氯化铁,1mol Fe失去电子数为3NA,故B正确;
C、依据氮原子质子数为7,氢原子质子数为1计算,1mol NH4+所含质子数为11NA,故C错误;
D、1 mol?L-1CaCl2溶液中,溶液体积不知,不能计算所含Ca2+离子的数目,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的条件应用,微粒结构分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
 下列不是高聚物(如图所示)的单体的是( )
下列不是高聚物(如图所示)的单体的是( )| A、CH2=CH-CN |
| B、CH2=CH-CH3 |
C、 |
| D、CH2=CH2 |
下列离子方程式书写正确的是( )
| A、Cl2与H2O反应:Cl2+H2O=2H++Cl-+ClO- |
| B、铁和足量稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| C、Al2(SO4)3溶液与氨水反应:Al3++3OH-=Al(OH)3↓ |
| D、Na与H2O反应:2Na+2H2O=2Na++2OH-+H2↑ |
下列各表述与示意图一致的是( )
A、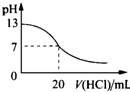 此图表示25℃时,用0.1mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 |
B、 此图表示一定条件下进行的反应2SO2(g)+O2(g)═2SO3(g)△H<0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 |
C、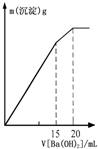 此图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
D、 此图表示化学反应H2(g)+C12(g)═2HCl(g)的能量变化,则该反应的反应热△H=﹢183kJ/mol |
下列装置或操作能达到实验目的是( )
A、 从a口进气可收集Cl2、NO2等气体 |
B、 在海带提碘实验中用于灼烧海带 |
C、 可用于吸收氨气能够防止倒吸 |
D、 用于分离互不相溶的液体混合物 |
皮肤上若沾上少量的苯酚,正确的处理方法是( )
| A、冷水冲洗 |
| B、用70℃以上热水冲洗 |
| C、用酒精擦洗 |
| D、用稀NaOH溶液清洗 |