题目内容
电解84.7mL质量分数为16%的氢氧化钠溶液(密度为1.18g?cm-3),过一段时间后,电解所得溶液中溶质的质量分数为19.5%(用石墨为电极),这是因为( )
| A、溶质增加了3.5 g |
| B、有1.5 mol水被电解 |
| C、在阳极生成2 g H2 |
| D、在阳极生成16 g O2 |
考点:电解原理
专题:电化学专题
分析:根据电解前后质量分数的变化可以计算电解掉的水的质量,电解氢氧化钠,溶剂减少,溶质质量不变,所以质量分数增大.
解答:
解:A、电解的实质是电解水,溶剂减少,溶质质量不变,故A错误;
B、电解的实质是电解水,溶剂减少,氢氧化钠的物质的量不变,设电解掉的水的质量是m,则84.7mL×1.18g/cm3×16%=19.5%×(84.7mL×1.18g/cm3-m),解得m≈18g,即1mol的水,所以水被电解了1mol,故B错误;
C、阳极氢氧根离子失去电子生成氧气,故C错误;
D、电解的实质是电解水,放出H2和O2,电解方程式为:2H2O
2H2↑+O2↑溶剂减少了18g,在阳极生成16g氧气,故D正确.
故选D.
B、电解的实质是电解水,溶剂减少,氢氧化钠的物质的量不变,设电解掉的水的质量是m,则84.7mL×1.18g/cm3×16%=19.5%×(84.7mL×1.18g/cm3-m),解得m≈18g,即1mol的水,所以水被电解了1mol,故B错误;
C、阳极氢氧根离子失去电子生成氧气,故C错误;
D、电解的实质是电解水,放出H2和O2,电解方程式为:2H2O
| ||
故选D.
点评:本题考查学生电解氢氧化钠的实质,明确电极反应是解题的关键,难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
做焰色反应实验用的铂丝,每次实验后必须进行的操作是( )
| A、用水洗涤2~3次 |
| B、用盐酸洗涤后,再用蒸馏水冲洗 |
| C、用滤纸擦拭干 |
| D、用盐酸洗涤后,再在酒精灯火焰上灼烧到没有其它颜色 |
能正确表示下列反应的离子方程式是( )
| A、钠投入水中:Na+H2O═Na++OH-+H2↑ |
| B、碳酸钙与醋酸反应:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
| C、少量碳酸氢钙溶液与足量氢氧化钠溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O |
| D、铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag |
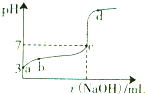 常温下,向20mL 0.1moL/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法不正确的是( )
常温下,向20mL 0.1moL/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法不正确的是( )| A、a点表示的溶液中c(OH-)=10-11mol/L | ||
B、a、b点表示的溶液中
| ||
| C、c点表示CH3COOH和NaOH恰好完全反应 | ||
| D、d点表示的溶液中c(Na+)>c(CH3COO-) |
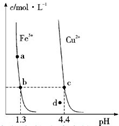 某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )
某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )| A、Ksp〔Fe (OH)3〕<Ksp〔Cu (OH)2〕 |
| B、加适量NH4Cl固体可使溶液由a 点变到b点 |
| C、c、d两点代表的溶液中c(H+) 与c(OH-)乘积相等 |
| D、Fe (OH)3、Cu (OH)2分别在b、c两点代表的溶液中达到饱和 |
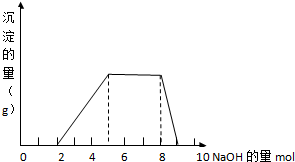 某溶液中可能含有H+,NH4+,Mg2+,Fe3+,Cl-,Al3+,SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:(已知:Fe3++3OH-=Fe(OH)3,且Fe(OH)3难溶于水;NH4++OH-=NH3?H2O)
某溶液中可能含有H+,NH4+,Mg2+,Fe3+,Cl-,Al3+,SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:(已知:Fe3++3OH-=Fe(OH)3,且Fe(OH)3难溶于水;NH4++OH-=NH3?H2O) ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: