题目内容
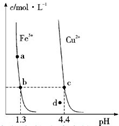 某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )
某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )| A、Ksp〔Fe (OH)3〕<Ksp〔Cu (OH)2〕 |
| B、加适量NH4Cl固体可使溶液由a 点变到b点 |
| C、c、d两点代表的溶液中c(H+) 与c(OH-)乘积相等 |
| D、Fe (OH)3、Cu (OH)2分别在b、c两点代表的溶液中达到饱和 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:根据图象找出可用来比较Fe(OH)3与Cu(OH)2溶度积常数点,可用b、c进行计算;由a点变到b点,PH增大,氯化铵水解呈酸性,不会增大溶液的PH;Kw只与温度有关;注意分析处在曲线上的点与曲线外的点有什么区别.
解答:
解:A、由b、c两点对应数据可比较出KSP[Fe(OH)3]与KSP[Cu(OH)2]的大小,KSP[Fe(OH)3]=c(Fe3+)?(OH-)3=c(Fe3+)?(10-12.7)3,
KSP[Cu(OH)2]=c(Cu2+)?(OH-)2=c(Cu2+)?(10-9.6)2,因c(Fe3+)=c(Cu2+),故KSP[Fe(OH)3]<KSP[Cu(OH)2],故A正确;
B、向溶液中加入NH4Cl固体,不会导致溶液中的c(OH-)增大,故不能使溶液由a点变到b点,故B错误;
C、只要温度不发生改变,溶液中c(H+)与c(OH-)的乘积(即Kw)就不变.该题中温度条件不变,故c、d两点代表的溶液中c(H+)与c(OH-)的乘积相等,故C正确;
D、b、c两点分别处在两条的沉淀溶解平衡曲线上,故两点均代表溶液达到饱和,故D正确.
故选B.
KSP[Cu(OH)2]=c(Cu2+)?(OH-)2=c(Cu2+)?(10-9.6)2,因c(Fe3+)=c(Cu2+),故KSP[Fe(OH)3]<KSP[Cu(OH)2],故A正确;
B、向溶液中加入NH4Cl固体,不会导致溶液中的c(OH-)增大,故不能使溶液由a点变到b点,故B错误;
C、只要温度不发生改变,溶液中c(H+)与c(OH-)的乘积(即Kw)就不变.该题中温度条件不变,故c、d两点代表的溶液中c(H+)与c(OH-)的乘积相等,故C正确;
D、b、c两点分别处在两条的沉淀溶解平衡曲线上,故两点均代表溶液达到饱和,故D正确.
故选B.
点评:本题考查了沉淀溶解平衡、溶度积、pH、水的离子积等,对图象中的数据进行定量或定性处理,找出数据(或坐标点)之间存在的相互关系;明确坐标点所表达的涵义;对溶度积和水的离子积有正确的理解.该题型重在考查综合能力,如分析(比较)、理解(转换)等.

练习册系列答案
相关题目
将15%的NaOH溶液蒸发掉100g水后得到125ml质量分数为30%的NaOH溶液,则此时溶液的物质的量浓度为( )
| A、6 mol?L-1 |
| B、6.25 mol?L-1 |
| C、6.75 mol?L-1 |
| D、7 mol?L-1 |
电解84.7mL质量分数为16%的氢氧化钠溶液(密度为1.18g?cm-3),过一段时间后,电解所得溶液中溶质的质量分数为19.5%(用石墨为电极),这是因为( )
| A、溶质增加了3.5 g |
| B、有1.5 mol水被电解 |
| C、在阳极生成2 g H2 |
| D、在阳极生成16 g O2 |
 已知 A、B、D是三种常见的有机物,相同条件下,A 的蒸气对于H2的相对密度为 23,A 可以被氧化成 B,E 是密度最小的气体,它们之间有如图所示的转化关系(反应条件及部分产物未标出).下列说法中错误的是( )
已知 A、B、D是三种常见的有机物,相同条件下,A 的蒸气对于H2的相对密度为 23,A 可以被氧化成 B,E 是密度最小的气体,它们之间有如图所示的转化关系(反应条件及部分产物未标出).下列说法中错误的是( )| A、A中的官能团是羟基 |
| B、反应①为取代反应,反应②为置换反应 |
| C、B能与CaCO3反应 |
| D、B与F不反应 |
下列有关实验的叙述正确的是( )
| A、只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 |
| B、用萃取分液的方法除去酒精中的水 |
| C、用可见光束照射以区别溶液和胶体 |
| D、根据火焰所呈现的特征焰色,只能检验金属离子的存在 |