题目内容
2.常温下,将20.0g 14.0%的NaCl溶液与30.0g 24.0%的NaCl溶液混合,得到密度为1.15g/cm3的混合液.水的密度为1g/cm3.(计算结果均须保留到小数点后面两位数字)(1)该混合溶液中溶质的质量分数;
(2)该溶液中溶质的物质的量浓度.
分析 (1)根据m(溶质)=m(溶液)×ω计算溶质的质量,计算混合后溶液的质量,利用混合后溶质的质量等于原不同浓度溶液中氯化钠的质量之和计算混合后溶质氢氧化质量分数;
(2)根据c=$\frac{1000ρω}{M}$计算混合液的物质的量浓度.
解答 解:(1)将20.0g14%的NaCl溶液跟30.0g24%的NaCl溶液混合,混合后溶液的质量为20g+30g=50g,
令混合后NaCl的质量分数为ω,则:50g×ω=20g×14%+30g×24%,解得ω=20%,
答:混合后NaCl溶液的质量分数为20%;
(2)混合后溶液中NaCl的物质的量浓度为$\frac{1000×1.15×20%}{58.5}$mol/L=3.93mol/L,
答:混合后氯化钠溶液的物质的量浓度为3.93mol/L.
点评 本题考查物质的量浓度、质量分数的有关计算,难度中等,注意对公式的理解与灵活运用,注意理解掌握物质的量浓度与质量分数之间关系.

练习册系列答案
相关题目
12.发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃刹.
(1)已知:2N2H4(1)+N2O4(1)═3N2(g)+4H2O(1)△H=-1225kJ•mol-1
断开1mol下列化学键吸收的能量分别为:N-H:391kJ;N-N:193kJ;N≡N:946kJ;O-H:463kJ.
则使1molN2O4(1)分子中化学键完全断裂时需要吸收的能量是1803KJ.
(2)t℃时,将一定量的NO2(g)和N2O4(g)充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
①c(X)代表NO2(填化学式)的浓度,该反应的平衡常数K=0.9;
②前10min内用NO2表示的反应速率为0.04mol/(L•min),20min时改变的条件是增大NO2的浓度(或向容器中加入0.8mol二氧化氮);重新达到平衡时,NO2的百分含量与原平衡状态相比B(填序号)
A.增大 B.减小 C.不变 D.无法判断
(3)肼的性质与氨相似,其水溶液显弱碱性.请用电离方程式表示肼的水溶液显碱性的原因:N2H4+H2O?N2H+5+OH-.肼与氧气构成的燃料电池在碱性条件下放电时,生成水与一种无污染的气体.放电时,该电池负极的电极反应式为N2H4+4OH--4e-=4H2O+N2.
(4)已知在相同条件下N2H4•H2O的电离程度大于N2H5Cl的水解程度.常温下,若将0.2mo1•L-1N2H4•H2O溶液与0.1mol•L-1HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
(1)已知:2N2H4(1)+N2O4(1)═3N2(g)+4H2O(1)△H=-1225kJ•mol-1
断开1mol下列化学键吸收的能量分别为:N-H:391kJ;N-N:193kJ;N≡N:946kJ;O-H:463kJ.
则使1molN2O4(1)分子中化学键完全断裂时需要吸收的能量是1803KJ.
(2)t℃时,将一定量的NO2(g)和N2O4(g)充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
| 时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/mol•L-1 | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/mol•L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10min内用NO2表示的反应速率为0.04mol/(L•min),20min时改变的条件是增大NO2的浓度(或向容器中加入0.8mol二氧化氮);重新达到平衡时,NO2的百分含量与原平衡状态相比B(填序号)
A.增大 B.减小 C.不变 D.无法判断
(3)肼的性质与氨相似,其水溶液显弱碱性.请用电离方程式表示肼的水溶液显碱性的原因:N2H4+H2O?N2H+5+OH-.肼与氧气构成的燃料电池在碱性条件下放电时,生成水与一种无污染的气体.放电时,该电池负极的电极反应式为N2H4+4OH--4e-=4H2O+N2.
(4)已知在相同条件下N2H4•H2O的电离程度大于N2H5Cl的水解程度.常温下,若将0.2mo1•L-1N2H4•H2O溶液与0.1mol•L-1HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
13.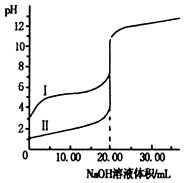 室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
 室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )| A. | I、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| B. | V(NaOH)=10.00mL时,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| C. | pH=7时,两种酸所消耗NaOH溶液的体积相等 | |
| D. | V(NaOH)=20.00mL时,c(Cl一)<c(CH3COO一) |
17.2016年10月17日,我国神舟11号飞船发射在即,长征三号丙型运载火箭开始加注燃料.长征三号丙型火箭第一级和第二级采用偏二甲肼(UDMH)和N2O4为动力源,反应方程式为:(CH3)2N2H2+2N2O4=2CO2+4H2O+3N2,关于该反应的说法中正确的是( )
| A. | 该反应不是氧化还原反应 | B. | 氮气只是氧化产物 | ||
| C. | N2O4是还原剂 | D. | N2O4是氧化剂 |