题目内容
10.一定条件下,在一个1L的密闭容器中,加入2mol A和1mol B,发生下列反应:2A(g)+B(g)?3C(g)+D(s),10min后达到平衡,平衡时C的浓度为0.12mol/L.(1)维持容器的温度不变,若缩小容器的体积,则平衡不移动(填“向正反应方向”或“向逆反应方向”或“不”).
(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍与上述平衡相同的是BC.
A.4mol A+2mol B
B.3mol C+1mol D
C.2mol A+1mol B+1mol D
(3)若维持容器内的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度与上述平衡相同,则C的起始物质的量应满足的条件是1.2mol<nc≤3mol.
(4)到达平衡时B的转化率为40%.若到达到平衡后向容器中加入少量的C,其它条件保持不变,B的转化率将变小(填“变大”或“变小”或“不变”).
分析 (1)对于反应前后体积不变的化学反应而言,压强变化不会引起化学平衡的移动;
(2)根据等效平衡判断即可;
(3)采用极限法求出C的物质的量;
(4)10min后达到平衡,平衡时C的浓度为0.12mol/L,结合方程式可计算消耗B的物质的量,以此计算B的转化率,加入少量C,平衡逆向移动.
解答 解:(1)D为固体,对于反应前后体积不变的化学反应,压强变化不会引起化学平衡的移动,
故答案为:不;
(2)根据等效平衡,把物质都换算成方程式一边的物质,且和初始加入的入2mol A和1mol B相等即可.
①4molA+2molB 与初始A、B浓度不同,故A错误;
②D是固体,量的多少不会引起化学平衡的移动,3molC换算成A、B,A、B浓度分别为2mol、1mol,与初始浓度相同,故B正确;
③D是固体,量的多少不会引起化学平衡的移动,2molA+1molB和题干投入量相等,故C正确.
故答案为:BC;
(3)若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol•L-1,此时和初始时是等效的,当加入2mol A和1mol B,即加入3molC,符合题意,如果假设C全部反应转化为A、B,此时C的物质的量最小是1.2mol,即1.2 mol<nc≤3mol,
故答案为:1.2 mol<nc≤3mol;
(4)10min后达到平衡,平衡时C的浓度为0.12mol/L,由方程式可知消耗B的物质的量为0.4mol,则B的转化率为$\frac{0.4mol}{1mol}×100%$=40%,由于容器的体积不变,加入少量C,生成物浓度增大,平衡逆向移动,B的转化率减小.
故答案为:40%; 变小.
点评 本题考查化学反应速率、化学平衡的有关计算、等效平衡等,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等,(2)中注意对等效平衡规律的理解.

 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径.目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H>0.
①写出该反应的平衡常数表达式K=$\frac{[CH{\;}_{3}OCH{\;}_{3}]•[H{\;}_{2}O]{\;}^{3}}{[CO{\;}_{2}]{\;}^{2}•[H{\;}_{2}]{\;}^{6}}$.
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是BD.
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2):v(H2)=1:3
D.容器内压强保持不变
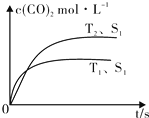
(2)汽车尾气净化的主要原理为:2NO(g)+2CO (g) $\stackrel{催化剂}{?}$2CO2 (g)+N2 (g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示.据此判断:
①该反应的△H<0(选填“>”、“<”).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(3)已知:CO(g)+2H2(g)?CH3OH(g)△H=-a kJ•mol-1.
①经测定不同温度下该反应的平衡常数如下:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |

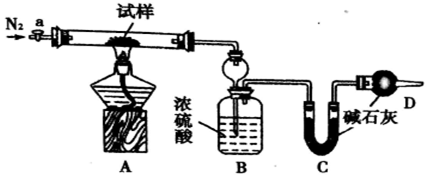
【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑
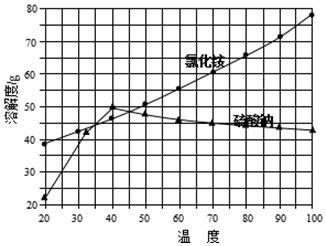
②氯化铵和硫酸钠的溶解度随温度变化曲线如图所示:
请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式:(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4.
(2)欲制备10.7g NH4Cl,理论上需NaCl质量为11.7g.
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有玻璃棒、烧杯、蒸发皿.
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为35℃.
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:
| 操作步骤 | 现象 | 结论 |
| 取少量氯化铵产品于试管底部,加热 | 如果试管底部没有固体剩余 | 表明氯化铵产品纯净 |
 麻黄素中含氧官能团的名称是羟基,属于醇类(填“醇”或“酚”).
麻黄素中含氧官能团的名称是羟基,属于醇类(填“醇”或“酚”).