题目内容
7.现有下列10种物质:①H2O②空气③Mg④CaO⑤H2SO4⑥Ca(OH)2⑦CuSO4.5H2O⑧碘酒⑨酒精⑩NaHCO3其中,属于混合物的是②⑧(填序号,下同);属于氧化物的是①④;属于酸的是⑤;属于碱的是⑥;属于盐的是⑦⑩;属于有机物的是⑨;属于电解质的是①④⑤⑥⑦⑩;属于非电解质的是⑨.
分析 由两种或以上物质构成的是混合物;
由两种元素构成,其中一种是氧元素的化合物为氧化物;
电离出的阳离子全部是氢离子的化合物为酸;
电离出的阴离子全部是氢氧根的化合物为碱;
电离出的阴离子是酸根离子、阳离子是金属离子或铵根离子的化合物为盐;
含碳元素的化合物为有机物;
在水溶液中或熔融状态下能导电的化合物为电解质;
在水溶液中和熔融状态下均不能导电的化合物为非电解质.据此分析.
解答 解:①H2O是氧化物,且为电解质;
②空气是混合物,既不是电解质也不是非电解质;
③Mg是单质,故既不是电解质也不是非电解质;
④CaO是氧化物,在熔融状态下能导电,故为电解质;
⑤H2SO4是酸,在水溶液中能导电,故为电解质;
⑥Ca(OH)2是碱,在水溶液中能导电,故为电解质;
⑦CuSO4.5H2O是盐,在水溶液中能导电,故为电解质;
⑧碘酒是碘单质和酒精组成的混合物,既不是电解质也不是非电解质;
⑨酒精是有机物,是非电解质;
⑩NaHCO3是盐,在水溶液中能导电,故为电解质.
故属于混合物的是②⑧;属于氧化物的是①④;属于酸的是 ⑤;属于碱的是 ⑥;属于盐的是 ⑦⑩;属于有机物的是 ⑨;属于电解质的是 ①④⑤⑥⑦⑩;属于非电解质的是⑨.
故答案为:②⑧;①④;⑤;⑥;⑦⑩;⑨; ①④⑤⑥⑦⑩;⑨.
点评 本题考查了电解质、非电解质和酸碱盐、氧化物的概念,掌握物质的成分和概念的要点是解题关键.

练习册系列答案
相关题目
18.以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠的工艺流程如图:

【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑
②氯化铵和硫酸钠的溶解度随温度变化曲线如图所示:
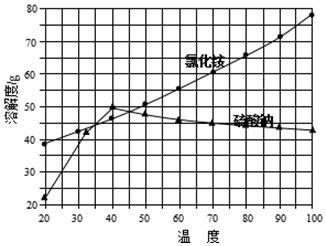
请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式:(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4.
(2)欲制备10.7g NH4Cl,理论上需NaCl质量为11.7g.
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有玻璃棒、烧杯、蒸发皿.
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为35℃.
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:

【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑
②氯化铵和硫酸钠的溶解度随温度变化曲线如图所示:

请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式:(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4.
(2)欲制备10.7g NH4Cl,理论上需NaCl质量为11.7g.
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有玻璃棒、烧杯、蒸发皿.
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为35℃.
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:
| 操作步骤 | 现象 | 结论 |
| 取少量氯化铵产品于试管底部,加热 | 如果试管底部没有固体剩余 | 表明氯化铵产品纯净 |
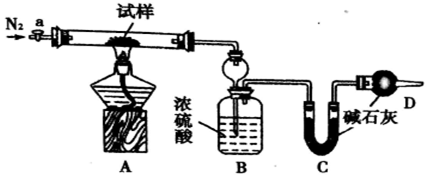
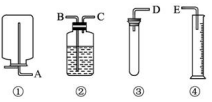 现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图
现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图