题目内容
5.最新研究表明:用CH4催化还原NO2可以消除氮氧化合物引起的污染,例如:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ/mol
下列说法正确的是( )
| A. | 等物质的量的CH4在反应①、②中转移的电子数不相同 | |
| B. | CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l);△H>-574kJ/mol | |
| C. | 4NO2(g)+2N2(g)═8NO(g);△H=+586kJ/mol | |
| D. | 若用2.24LCH4把NO2还原为N2,整个过程中转移的电子总数为0.8NA |
分析 A.根据化合价升高数=化合价降低数=转移电子数来回答;
B.气态水转变为液态水要放热;
C.根据反应①②,利用盖斯定律结合热化学方程式系数的意义来回答;
D.没有说明是否是标准状况下,无法计算.
解答 解:A.反应①②转移的电子数=化合价升高数=化合价降低数=8,反应甲烷中C元素的化合价升高8价,转移8个 电子,则转移电子相同,故A错误;
B.因为气态水转变为液态水要放热,所以由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H<-574kJ•mol-1,故B错误;
C.由反应①②,利用盖斯定律,反应4NO2(g)+2N2(g)═8NO(g),可以是(①-②)得到,所以该反应的△H=(-574kJ/mol+1160kJ/mol)=+586kJ/mol,故C正确;
D.没有说明是否是标准状况下,气体的摩尔体积不知道,无法计算甲烷的物质的量,即无法计算转移的电子,故D错误;
故选C.
点评 本题考查学生热化学方程式的含义以及化学方程式、电子转移知识,属于综合知识的考查,难度中等,注意从化合价的角度分析电子转移,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
15.O3在水中易分解生成O2,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示.已知:O3的起始浓度为0.02mol•L-1.
(1)pH增大能加速(填“加速”或“减缓”)O3分解,其中对O3分解起催化作用的是OH-(填“OH-”或“H+”).
(2)在30℃、pH=5.0条件下,O3的分解速率为2.00×10-4 mol•L-1•min-1,O2的浓度为0.015mol/L.
(3)据表中的递变规律,推测O3在下列条件下分解速率的关系:Ⅰ<(填“>”“<”或“=”)Ⅱ.
Ⅰ.40℃,pH=3.0
Ⅱ.30℃,pH=7.0.
| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 300 | 230 | 169 | 58 |
| 30 | 158 | 108 | 50 | 15 |
| 50 | 31 | 26 | 15 | 7 |
(2)在30℃、pH=5.0条件下,O3的分解速率为2.00×10-4 mol•L-1•min-1,O2的浓度为0.015mol/L.
(3)据表中的递变规律,推测O3在下列条件下分解速率的关系:Ⅰ<(填“>”“<”或“=”)Ⅱ.
Ⅰ.40℃,pH=3.0
Ⅱ.30℃,pH=7.0.
13.下列关于铯(Cs)及其化合物的性质的说法中,正确的是( )
| A. | 金属铯的密度比金属钠小 | B. | 金属铯的熔点比金属钠高 | ||
| C. | Cs与H2O能剧烈反应,甚至发生爆炸 | D. | 碳酸铯难溶于水 |
20.10mL某种气态烃,在50mL氧气中完全燃烧,得到液态水和体积为35mL的混合气体(所有气体体积都是在同温同压下测定),则下列烃中符合题意的烃是( )
| A. | CH4 | B. | C2H2 | C. | C3H8 | D. | C2H6 |
10.常温下.弱碱MOH的电离常数K=1.0×10-3,0.1mol•L-1 MOH溶液的pH约为( )
| A. | 8 | B. | 9 | C. | 11 | D. | 12 |
17.高铁酸钾K2FeO4是一种高效、氧化性比Cl2更强的水处理剂,工业上常用下列反应先制高铁酸钠:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,然后在低温下,在Na2FeO4溶液中加KOH固体至饱和就可析出K2FeO4,下列有关说法不正确的是( )
| A. | Na2O2在反应中作氧化剂,又作还原剂 | |
| B. | 高铁酸钾在该温度下的溶解度比高铁酸钠的溶解度小 | |
| C. | K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮物 | |
| D. | 制取高铁酸钠时,每生成1mol Na2FeO4反应中共有4mol电子转移 |
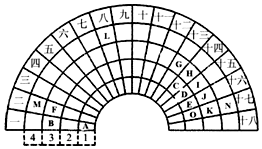 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题: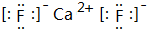 ,用电子式表示CJ2的形成过程:
,用电子式表示CJ2的形成过程: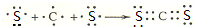 .
.