��Ŀ����
19������ƽ����ϵmA��g��+nB��g��?pC��g��+gD��g������H��0�����н����д�����ǣ�������| A�� | ���¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������m+n��p+q | |
| B�� | ���¶Ȳ��䣬ѹǿ����ԭ����2�����ﵽ��ƽ��ʱ�������һ����ԭ����$\frac{1}{2}$ҪС | |
| C�� | ��m+n=p+q����������a mol�����ƽ����ϵ���ټ���a mol��B���ﵽ��ƽ��ʱ������������ʵ�������2a | |
| D�� | ��ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n |
���� A�����¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������֪����ѹǿ��ƽ�������ƶ���
B��m+n=p+qʱ��ѹǿ����ԭ����2�������������Ϊԭ����$\frac{1}{2}$��
C����m+n=p+q����֪��Ӧǰ����������ʵ������䣻
D����ƽ��ʱ��A��B��ת������ȣ�����ʼ���ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�
��� �⣺A�����¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������֪����ѹǿ��ƽ�������ƶ�����m+n��p+q����A��ȷ��
B��m+n=p+qʱ��ѹǿ����ԭ����2�������������Ϊԭ����$\frac{1}{2}$����m+n��p+qʱ��ѹǿ����ԭ����2�����ﵽ��ƽ��ʱ���������ԭ����$\frac{1}{2}$ҪС����B����
C����m+n=p+q����֪��Ӧǰ����������ʵ������䣬��������a mol�����ƽ����ϵ���ټ���a mol��B���ﵽ��ƽ��ʱ������������ʵ�������2a����C��ȷ��
D����ƽ��ʱ��A��B��ת������ȣ�����ʼ���ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n����D��ȷ��
��ѡB��
���� ���⿼�黯ѧƽ����ƶ���Ϊ��Ƶ���㣬�����¶ȡ�Ũ�ȡ�ѹǿ��ƽ���ƶ���Ӱ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע������Ļ�ѧ�������Ĺ�ϵ����Ŀ�ѶȲ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���һ���Ʊ�����ϩ��ԭ���練ӦI��ʾ����
I��
 ��H=+124kJ•mol-1
��H=+124kJ•mol-1��1�����ֻ�ѧ���ļ��������ʾ��
| ��ѧ�� | C-H | C-C | C�TC | H-H |
| ����/kJ•mol-1 | 412 | 348 | x | 436 |
��2����ҵ�ϣ��ں�ѹ�豸�н��з�ӦIʱ�������ұ�������ͨ��һ������ˮ�������û�ѧƽ�����۽���ͨ��ˮ������ԭ��Ϊ����ӦΪ�������������ķ�Ӧ������ѹǿ���䣬����ˮ�������������Ӧ����ЧΪ����ѹǿ��ƽ��������Ӧ�����ƶ�������ұ���ƽ��ת���ʣ�
��3������ϵ�����ܱ仯�ĽǶȷ�������ӦI�ڸ��£�����¡����¡��������������Է����У�
�������Ʊ���-���һ�����ԭ���練ӦII��ʾ����
II��
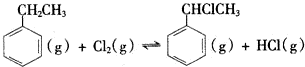 ��H2��0
��H2��0��4��T��ʱ����10L�����ܱ������г���2mol�ұ���g����2mol Cl2��g��������Ӧ��5minʱ�ﵽƽ�⣬�ұ���Cl2�����ʵ���Ũ�ȣ�c����ʱ�䣨t���仯��������ͼl��ʾ��

��0-5min�ڣ���HC1��ʾ�ĸ÷�Ӧ����v��HCl��=0.032 mol•L-1•min-1��
��T��ʱ���÷�Ӧ��ƽ�ⳣ��K=16��
��6minʱ���ı���������Ϊ�����¶ȣ�
��10minʱ�����������������䣬���������г���1moI�ұ���1mol Cl2��1mol ��-���һ�����l mol HCl��12minʱ�ﵽ��ƽ�⣮��ͼ2�л���10-12 min��Cl2��HCl��Ũ�ȱ仯���ߣ������ϱ���Cl2��HCl����0-5min��0-12minʱ��Σ�Cl2��ת���ʷֱ��æ�1����2 ��ʾ�����l����2�����������������=������
��1����һ���¶��£��ڹ̶�������ܱ������н��п��淴Ӧ��N2+3H2?2NH3 �ÿ��淴Ӧ�ﵽƽ��ı�־��BCE��
A��3v��H2����=2v��NH3����
B����λʱ������m mol N2��ͬʱ����3m mol H2
C�������ڵ���ѹǿ������ʱ����仯
D�����������ܶȲ�����ʱ����仯
E��a mol N��N�����ѵ�ͬʱ����6a mol N-H������
F��N2��H2��NH3�ķ�����֮��Ϊ1��3��2
��2��ij��ѧ�о���ѧϰС��ģ�ҵ�ϳɰ��ķ�Ӧ�����ݻ��̶�Ϊ2L���ܱ������ڳ���1mol N2��3mol H2��������ʴ�����������Ժ��Բ��ƣ�����һ���¶�ѹǿ�¿�ʼ��Ӧ������ѹ���Ƽ��������ѹǿ�ı仯�����
| ��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
���¶���ƽ�ⳣ��K=2.37��
| A�� | ���д������ڵ������£���Ӧ�ų�������Ϊ92.4 kJ | |
| B�� | �������÷�Ӧ�ų���������Ϊ92.4 kJ | |
| C�� | ���ٳ���1 mol H2������ƽ��ʱ�ų�������ӦΪ92.4 kJ | |
| D�� | ��Ӧ�ų�������ʼ��С��92.4 kJ |
��2����ȡ��Ӧ��ʱ��ȡ50mL 0.50mol•L-1�����ᣬ���������Լ���B��
A��50mL 0.50mol•L-1 NaOH��Һ B��50mL 0.55mol•L-1 NaOH��Һ
C��1.0g NaOH����
��3��ʵ��ʱ���ձ���������Ӳֽ�壬��õ��к�����ֵƫС����ƫ��ƫС����Ӱ�죩
��4���ɼס���������ɵ�ʵ��С�飬��ͬ����ʵ�������£���ͬ����ʵ�������ͷ�����������ⶨ�к��ȵ�ʵ�飬ʵ���Լ��������������ʾ��
| ��Ӧ�� | ��ʼ�¶�t1/�� | �����¶�t2/�� | �к���/kJ•mol-1 |
| A.1.0mol/L HCl��Һ50mL��1.1mol/L NaOH��Һ50mL | 13.0 | 19.8�� | ��H1 |
| B.1.0mol/L HCl��Һ50mL��1.1mol/L NH3•H2O��Һ50mL | 13.0 | 19.3�� | ��H2 |
�ڡ�H1�١�H2ԭ����NaOH��ǿ�NH3•H2O������������ȣ�
��1��Fe��ԭˮ����NO3-�ķ�Ӧԭ����ͼ1��ʾ��

��������������������
�������ĵ缫��Ӧʽ��NO3-+8e-+10H+=NH4++3H2O��
��2������������Ͷ��ˮ���У���24Сʱ�ⶨNO3-��ȥ���ʺ�pH����������
| ��ʼpH | pH=2.5 | pH=4.5 |
| NO3-��ȥ���� | �ӽ�100% | ��50% |
| 24СʱpH | �ӽ����� | �ӽ����� |
| ��������������̬ |  |  |
��3��ʵ�鷢�֣��ڳ�ʼpH=4.5��ˮ����Ͷ���������۵�ͬʱ������һ������Fe2+�����������NO3-��ȥ���ʣ���Fe2+������������ּ��裺
��Fe2+ֱ�ӻ�ԭNO3-��
��Fe2+�ƻ�FeO��OH�������㣮
�����Ա�ʵ�飬�������ͼ2��ʾ���ɵõ��Ľ����DZ�ʵ�������£�Fe2+����ֱ�ӻ�ԭNO3-����Fe��Fe2+��ͬ�����������NO3-��ȥ���ʣ�
��ͬλ��ʾ�ٷ�֤ʵFe2+����FeO��OH����Ӧ����Fe3O4����ϸ÷�Ӧ�����ӷ���ʽ�����ͼ���Fe2+���NO3-ȥ���ʵ�ԭ��Fe2++2FeO��OH��=Fe3O4+2H+��Fe2+���������FeO��OH��ת��Ϊ�ɵ����Fe3O4�����ڵ���ת�ƣ�pH=4.5������������ͬ��
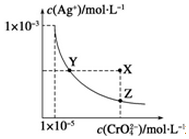 ��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgBr��Ksp=5.0��10-13������˵��������ǣ�������
��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgBr��Ksp=5.0��10-13������˵��������ǣ�������| A�� | t��ʱ��Ag2CrO4��KspΪ1��10-8 | |
| B�� | �ڱ���Ag2CrO4��Һ�м���K2CrO4����ʹ��Һ��Y���ΪX�� | |
| C�� | һ���¶���Y���Z��ʱAg2CrO4��Ksp��� | |
| D�� | ��t��ʱ��Ag2CrO4��s��+2Br-��aq��?2AgBr��s��+CrO42-��aq��ƽ�ⳣ��K=4.0��1010 |