题目内容
1.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验.甲同学:向1mol•L-1的氯化铁溶液中加入少量的NaOH溶液.
乙同学:直接加热饱和FeCl3溶液.
丙同学:向25mL沸水中遂滴加入5〜6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热.试回答下列问题:
(1)其中操作正确的同学是丙(填“甲”“乙”或“丙”).
(2)涉及到的化学方程式是FeCl3+3H2O═Fe(OH)3(胶体)+3HCl.
(3)证明有Fe(OH)3胶体生成的实验操作是用激光笔照射,若有一条光亮的通路,则有胶体生成,此现象利用了胶体的一种性质,称为丁达尔效应.
(4)向制得的Fe(OH)3,胶体中加入饱和的琉酸铵溶液,产生沉淀原因是氢氧化铁胶粒带正电,遇硫酸铵溶液发生胶体的聚沉,若逐滴加入稀硫酸至过量,产生的现象先生成红褐色的沉淀,后溶解为黄色溶液.
分析 (1)制备氢氧化铁胶体的方法:向25ml沸水中逐滴加入1~2mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,加热会促进胶体聚沉;
(2)氯化铁水解生成氢氧化铁胶体;
(3)胶体的特有的性质为丁达尔效应;
(4)胶体遇电解质溶液能发生聚沉得到氢氧化铁沉淀,继续滴加硫酸,氢氧化铁沉淀溶解.
解答 解:(1)甲同学向1mol•L-氯化铁溶液中加入少量的NaOH溶液,会发生复分解反应生成红褐色沉淀,乙同学直接加热饱和FeCl3溶液,三价铁会水解生成红褐色沉淀,制备氢氧化铁胶体的方法:向25ml沸水中逐滴加入1~2mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,故答案为:丙;
(2)氯化铁水解生成氢氧化铁胶体,化学方程式:FeCl3+3H2O═Fe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2O═Fe(OH)3(胶体)+3HCl;
(3)丁达尔效应是胶体的特有性质,可用来鉴别胶体,当用激光笔照射时,会有一道明亮的光路,
故答案为:用激光笔照射,若有一条光亮的通路,则有胶体生成;丁达尔效应;
(4)向氢氧化铁胶体中胶粒带正电,当逐滴加饱和的硫酸铵溶液后,会发生胶体的聚沉;当入过量H2SO4溶液,H2SO4电离出的SO42-使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解,会观察到先出现红褐色沉淀,后沉淀消失.
故答案为:氢氧化铁胶粒带正电,遇硫酸铵溶液发生胶体的聚沉;先生成红褐色的沉淀,后溶解为黄色溶液.
点评 本题考查胶体的制备、性质,题目难度不大,易错点为胶体的制备,注意制备方法,本题重点把握胶体的聚沉的性质.

练习册系列答案
相关题目
16.下列仪器经常用于物质分离的有( )
①漏斗②试管③蒸馏烧瓶④天平⑤分液漏斗⑥容量瓶⑦蒸发皿⑧坩埚.
①漏斗②试管③蒸馏烧瓶④天平⑤分液漏斗⑥容量瓶⑦蒸发皿⑧坩埚.
| A. | ①③⑤⑥ | B. | ①②④⑥ | C. | ①③⑤⑦ | D. | ①③⑤⑧ |
6.下列关于电解槽的叙述中不正确的是( )
| A. | 与电源正极相连的是电解槽的阴极 | |
| B. | 与电源负极相连的电极发生还原反应 | |
| C. | 在电解槽的阳极发生氧化反应 | |
| D. | 电子从电源的负极沿导线流入阴极 |
13.20世纪90年代,国际上提出了“预防污染”的新概念.“绿色化学”是预防污染的基本手段,下列各项中属于“绿色化学”的是( )
| A. | 对燃烧煤时产生的尾气进行除硫处理 | |
| B. | 往已经酸化的土壤撒石灰中和 | |
| C. | 煤燃烧时鼓入足量空气 | |
| D. | 将煤除硫后再燃烧 |
19.对于平衡体系mA(g)+nB(g)?pC(g)+gD(g);△H<0.下列结论中错误的是( )
| A. | 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q | |
| B. | 若温度不变,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的$\frac{1}{2}$要小 | |
| C. | 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a | |
| D. | 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用.请回答下列问题:
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用.请回答下列问题: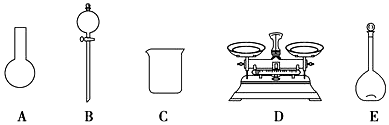

 .
.