题目内容
13.下列化合物中,既含有离子键又含有共价键的是( )| A. | NaNO3 | B. | MgO | C. | C2H6 | D. | CO2 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.NaNO3中Na+与NO3-之间以离子键结合,NO3-内部原子之间以共价键结合,故A选;
B.MgO中含镁离子和氧负离子之间的离子键,故B不选;
C.C2H6中只含共价键,故C不选;
D.CO2中只含共价键,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
3.对于在一定条件下进行的化学反应:2SO2+O2?2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是( )
| A. | 升高温度 | B. | 增大压强 | C. | 减小反应物浓度 | D. | 增大反应物浓度 |
1.已知:①2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列说法中错误的是( )
②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列说法中错误的是( )
| A. | ①式表示常温常压时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ | |
| B. | 2H2(g)+O2(g)=2H2O(g)中△H大于-571.6 kJ•mol-1 | |
| C. | 将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量大于57.3 kJ | |
| D. | 将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量为57.3 kJ |
18.下列物质中,能与氢氧化钠溶液反应,但不与盐酸反应的是( )
| A. | Al(OH)3 | B. | Al2O3 | C. | SiO2 | D. | Al |
5.某离子M2+含有a个中子,质量数为m,则电子数为( )
| A. | a-2 | B. | a+2 | C. | m-a+2 | D. | m-a-2 |
2.BF3与一定量的水形成晶体Q[(H2O)2•BF3],Q在一定条件下可转化为R:

晶体Q中各种微粒间的作用力不涉及( )
①离子键 ②共价键 ③配位键 ④金属键 ⑤氢键 ⑥范德华力.

晶体Q中各种微粒间的作用力不涉及( )
①离子键 ②共价键 ③配位键 ④金属键 ⑤氢键 ⑥范德华力.
| A. | ①⑤ | B. | ②⑥ | C. | ①④ | D. | ①④⑥ |
3.下列措施对增大反应速率明显有效的是( )
| A. | 钾与水反应时增大水的用量 | |
| B. | 铝与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | 实验室制取二氧化碳时,将块状大理石改为粉状大理石 |
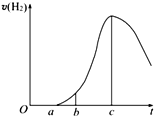 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题: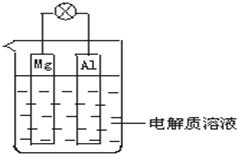 如图所示,试回答下列问题 (灯泡功率合适):
如图所示,试回答下列问题 (灯泡功率合适):