题目内容
18.由W、X、Y、Z四种金属按下列装置进行实验.下列说法不正确的是( )| 装置 |  | 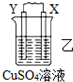 |  |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体发生 |
| A. | 装置甲中W作原电池负极 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH减小 | |
| D. | 四种金属的活动性强弱顺序为Z>W>X>Y |
分析 A.负极失电子逐渐溶解;
B.Y上铜离子得电子生成Cu;
C.W上氢离子得电子生成氢气,溶液中氢离子浓度减小;
D.负极的活泼性大于正极.
解答 解:A.装置甲中金属W不断溶解,负极失电子逐渐溶解,则W作原电池负极,故A正确;
B.Y上铜离子得电子生成Cu,则Y电极上的反应式为Cu2++2e-=Cu,故B正确;
C.W上氢离子得电子生成氢气,溶液中氢离子浓度减小,所以溶液的pH增大,故C错误;
D.甲中W为负极,X为正极,则活动性:W>X;乙中X为负极,Y为正极,则活动性:X>Y;丙中Z为负极,W为正极,则活动性:Z>W,所以四种金属的活动性强弱顺序为Z>W>X>Y,故D正确;
故选C.
点评 本题考查原电池知识,题目难度不大,注意把握原电池中正负极的判断方法以及电极方程式的书写方法,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.XY2是离子化合物,X和Y离子的电子层结构都与氖原子相同,则X、Y为( )
| A. | Ca和Cl | B. | K和S | C. | Ca和F | D. | Mg和F |
9.在AlCl3和FeCl3的混合液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得到的沉淀物是( )
| A. | Fe2S3、I2 | B. | FeS、S、Al(OH)3 | C. | Al(OH)3、I2 | D. | Fe(OH)3、Al(OH)3 |
13.在有机物的反应中,我们又学习到了新的反应类型,如取代反应,加成反应等,下列对反应类型的描述正确的是( )
| A. | 苯与浓硝酸在浓硫酸作用下共热至50~60℃属于加成反应 | |
| B. | 乙烯通入溴水中,使溴水褪色属于取代反应 | |
| C. | 苯在一定条件和氢气反应,属于加成反应 | |
| D. | 乙烯和水在一定条件下反应生成乙醇属于氧化反应 |
3.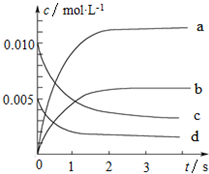 800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.
800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.
(1)从0~3s内,用NO表示的平均反应速率v(NO)=2.17×10-3mol•L-1•s-1.
(2)图中表示NO浓度变化的曲线是c(填字母代号).
(3)达平衡时NO的转化率为65%.
(4)能说明该反应已达到平衡状态的是ACD(填序号).
A.混合气体的颜色保持不变
B.混合气体的密度保持不变
C.v逆 (NO2)=2v正 (O2)
D.混合气体的平均相对分子质量保持不变
(5)若升温到850℃,达平衡后n(NO)=n(NO2),则反应向逆反应方向(填“正反应方向”“逆反应方向”)移动.
(6)若在一定条件下0.2molNO气体与氧气反应,达平衡时测得放出的热量为akJ,此时NO转化率为80%,则2molNO气体完全反应放出的热量为12.5akJ.
 800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.
800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.| 时间∕s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)∕mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO浓度变化的曲线是c(填字母代号).
(3)达平衡时NO的转化率为65%.
(4)能说明该反应已达到平衡状态的是ACD(填序号).
A.混合气体的颜色保持不变
B.混合气体的密度保持不变
C.v逆 (NO2)=2v正 (O2)
D.混合气体的平均相对分子质量保持不变
(5)若升温到850℃,达平衡后n(NO)=n(NO2),则反应向逆反应方向(填“正反应方向”“逆反应方向”)移动.
(6)若在一定条件下0.2molNO气体与氧气反应,达平衡时测得放出的热量为akJ,此时NO转化率为80%,则2molNO气体完全反应放出的热量为12.5akJ.
7.日常所用锌-锰干电池的电极分别为锌筒和石墨棒,以糊状NH4Cl作电解质,电极反应为:Zn-2e-=Zn2+,2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.有关锌-锰干电池的叙述中,正确的是( )
| A. | 锌-锰干电池中锌筒为正极,石墨棒为负极 | |
| B. | 锌-锰干电池即使不用,放置过久,也会失效 | |
| C. | 锌-锰干电池工作时,电流方向是由锌筒经外电路流向石墨棒 | |
| D. | 锌-锰干电池可实现化学能向电能和电能向化学能的相互转化 |
8.化学与生活是紧密相连的,下列说法正确的是( )
| A. | 食用油脂饱和程度越大,熔点越高 | |
| B. | 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 | |
| C. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| D. | 用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的氧化性 |


 CH3COOCH2CH3+H2O,用饱和碳酸钠溶液(填药品名称) 收集粗产品,用分液(填操作名称)的方法把粗产品分离.
CH3COOCH2CH3+H2O,用饱和碳酸钠溶液(填药品名称) 收集粗产品,用分液(填操作名称)的方法把粗产品分离.