题目内容
3.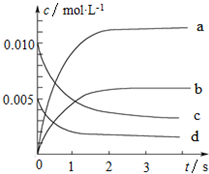 800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.
800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)?2NO2,n(NO)随时间的变化如表所示.| 时间∕s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)∕mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO浓度变化的曲线是c(填字母代号).
(3)达平衡时NO的转化率为65%.
(4)能说明该反应已达到平衡状态的是ACD(填序号).
A.混合气体的颜色保持不变
B.混合气体的密度保持不变
C.v逆 (NO2)=2v正 (O2)
D.混合气体的平均相对分子质量保持不变
(5)若升温到850℃,达平衡后n(NO)=n(NO2),则反应向逆反应方向(填“正反应方向”“逆反应方向”)移动.
(6)若在一定条件下0.2molNO气体与氧气反应,达平衡时测得放出的热量为akJ,此时NO转化率为80%,则2molNO气体完全反应放出的热量为12.5akJ.
分析 (1)由表格中数据可知,0~3s内,△n(NO)=(0.020-0.007)mol=0.013mol,带人v=$\frac{△n}{V•△t}$计算;
(2)NO和O2为反应物,随着时间的推移,NO和O2的物质的量逐渐减小,△n(NO):△n(O2)=2:1;
(3)3s时处于平衡状态,平衡时NO为0.007mol,NO转化率=$\frac{反应的NO物质的量}{NO起始物质的量}$×100%;
(4)A.混合气体的颜色保持不变,说明NO2的浓度保持恒定;
B.由$ρ=\frac{m}{V}$可知混合气体的密度始终保持不变;
C.因为$\frac{{v}_{正}({O}_{2})}{{v}_{正}(N{O}_{2})}=\frac{1}{2}$,所以v逆 (NO2)=2v正 (O2)=v正 (NO2);
D.根据M=$\frac{m}{n}$分析混合气体的平均相对分子质量是否为定值;
(5)升温到850℃,平衡后n(NO)=n(NO2),根据N原子守恒可知n(NO)=n(NO2)=0.1mol,平衡向逆反应进行;
(6)由题意可知转化的NO为0.16mol,放出的热量为akJ,所以2molNO反应放出的热量为12.5aKJ.
解答 解:(1)由表格中数据可知,0~3s内,△n(NO)=(0.020-0.007)mol=0.013mol,v(NO)=$\frac{0.013mol/L}{2L×3s}$=2.17×10-3mol•L-1•s-1,
故答案为:2.17×10-3mol•L-1•s-1;
(2)(2)NO和O2为反应物,随着时间的推移,NO和O2的物质的量逐渐减小,△c(NO):△c(O2)=2:1,因此c表示NO浓度变化的曲线,d表示O2浓度变化的曲线,
故答案为:c;
(3)3s时处于平衡状态,平衡时NO为0.007mol,NO转化率=$\frac{反应的NO物质的量}{NO起始物质的量}$×100%=$\frac{0.013}{0.020}$×100%=65%,
故答案为:65%;
(4)A.混合气体的颜色保持不变,说明NO2的浓度保持恒定,说明该反应已达到平衡状态;
B.由$ρ=\frac{m}{V}$可知混合气体的密度始终保持不变,不能说明该反应已达到平衡状态;
C.因为$\frac{{v}_{正}({O}_{2})}{{v}_{正}(N{O}_{2})}=\frac{1}{2}$,所以v逆 (NO2)=2v正 (O2)=v正 (NO2),说明该反应已达到平衡状态;
D.根据M=$\frac{m}{n}$,m是定值,n是变量,所以M为变量,因此混合气体的平均相对分子质量保持不变,说明该反应已达到平衡状态;
故答案为:ACD;
(5)升温到850℃,平衡后n(NO)=n(NO2),根据N原子守恒可知n(NO)=n(NO2)=0.1mol,平衡向逆反应进行,
故答案为:逆反应方向;
(6)转化的NO的物质的量为2mol×80%=0.16mol,放出的热量为akJ,所以2molNO反应放出的热量为$\frac{2mol}{0.16mol}$×akJ=12.5aKJ,
故答案为:12.5akJ.
点评 考查反应速率、平衡移动、平衡状态判断,热化学方程式等,旨在考查学生对基础知识的掌握理解,难度中等,加强化学反应原理的应用能力.

 阅读快车系列答案
阅读快车系列答案| A. | H2和D2互为同素异形体 | B. | 正丁烷和异丁烷是同系物 | ||
| C. |  和 和 互为同分异构体 互为同分异构体 | D. |  和 和  是同一种物质 是同一种物质 |
| A. | 该有机物分子中不含有氧原子 | B. | 该有机物分子中含一个氧原子 | ||
| C. | 该有机物一个分子中含2个氧原子 | D. | 该物质结构简式为CH3CHO |
| A. | C3H6和C5H10 | B. | CH3CH(CH3)CH2CH3和CH3C(CH3)3 | ||
| C. | C2H6和C4H10 | D. | C2H4和CH2=CH-CH=CH2 |
| 装置 |  |  |  |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体发生 |
| A. | 装置甲中W作原电池负极 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH减小 | |
| D. | 四种金属的活动性强弱顺序为Z>W>X>Y |
| A. | 2H2+O2═2H2O△H=-484 kJ•mol-1 | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242 kJ | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=+242 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-484 kJ•mol-1 |
| A. | 熔点:Li<Na<K | B. | 熔沸点:Al>Mg | C. | 密度:Na>Mg>Al | D. | 硬度:Mg<K |
| A. | 苯、己烷、四氯化碳 | B. | 苯、乙醇、四氯化碳 | ||
| C. | 植物油、乙醇、乙酸乙酯 | D. | 乙酸乙酯、乙醇、乙酸 |