题目内容
7.日常所用锌-锰干电池的电极分别为锌筒和石墨棒,以糊状NH4Cl作电解质,电极反应为:Zn-2e-=Zn2+,2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.有关锌-锰干电池的叙述中,正确的是( )| A. | 锌-锰干电池中锌筒为正极,石墨棒为负极 | |
| B. | 锌-锰干电池即使不用,放置过久,也会失效 | |
| C. | 锌-锰干电池工作时,电流方向是由锌筒经外电路流向石墨棒 | |
| D. | 锌-锰干电池可实现化学能向电能和电能向化学能的相互转化 |
分析 A、干电池中较活泼的金属作负极,较不活泼的导电的非金属作正极;
B、干电池中的电解质溶液易与锌反应减小电解质的量和电极材料的量干电池工作时,
C、电流从正极经外电路流向负极;
D、干电池是一次电池.
解答 解:A、干电池中较活泼的金属锌作负极,较不活泼的导电的非金属碳作正极,故A错误;
B、干电池中的电解质溶液易与锌反应减小电解质的量和电极材料的量,所以锌锰干电池即使不用,长久放置也会失效,故B正确;
C、干电池工作时,电流由正极碳经外电路流向负极锌,故C错误;
D、干电池是一次电池,所以不能实现化学能与电能的相互转化,故D错误;
故选B.
点评 本题考查了干电池的工作原理,难度不大,明确干电池和蓄电池的区别.

练习册系列答案
相关题目
17.下列叙述中正确的是面( )
| A. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成2,4,6三溴苯酚,再过滤除去 | |
| B. | 将苯酚晶体放入少量水中,加热时全部溶解,冷却到50℃时,溶液仍保持澄清 | |
| C. | 苯酚的酸性很弱,不能使指示剂变色,但可以与NaHCO3溶液反应放出CO2 | |
| D. | 苯酚可以与浓硝酸发生硝化反应 |
18.由W、X、Y、Z四种金属按下列装置进行实验.下列说法不正确的是( )
| 装置 |  | 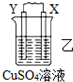 |  |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体发生 |
| A. | 装置甲中W作原电池负极 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH减小 | |
| D. | 四种金属的活动性强弱顺序为Z>W>X>Y |
2.以下实验能获得成功的是( )
| A. | 用酸性KMnO4溶液鉴别乙烯和乙炔 | |
| B. | 将铁屑、液溴、苯混合制溴苯 | |
| C. | 苯和溴苯采用分液的方法分离 | |
| D. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ |
12.下列对各组物质性质的比较中,正确的是( )
| A. | 熔点:Li<Na<K | B. | 熔沸点:Al>Mg | C. | 密度:Na>Mg>Al | D. | 硬度:Mg<K |
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 30g乙烷中所含的极性共价键数为7NA | |
| B. | 标准状况下,22.4LN2和CO2混合气体所含的分子数为2NA | |
| C. | 1L浓度为1mol•L-1的H2O2水溶液中含有的氧原子数为2NA | |
| D. | MnO2和浓盐酸反应生成1mol氯气时,转移电子数为2NA |
9.可以用于鉴别Fe、C、Cu0、Mn02四种黑色固体的一种试剂是( )
| A. | 稀H2SO4 | B. | 浓HCl | C. | 稀HCl | D. | 氯水 |