籾朕坪否
8⤴厮岑W、X、Y、Z、R頁玉巓豚嶄圻徨會方卆肝奐寄議5嶽麼怛圷殆⇧凪嶄W、Z揖怛⇧拝圻徨會方屢餓8⇧圷殆X壓揖巓豚議麼怛圷殆嶄圻徨磯抄恷寄⇧Y頁仇診嶄根楚恷謹議署奉圷殆⤴和双傍隈嶄屎鳩議頁↙ ⇄| A⤴ | 賑蓑狽晒麗糧協來⦿R﹅Z﹅W | |
| B⤴ | 圻徨磯抄⦿R〽W〽Y〽Z〽X | |
| C⤴ | X蛍艶嚥W、R侘撹議晒栽麗議晒僥囚窃侏音匯協屢揖 | |
| D⤴ | 窮盾X嚥R侘撹晒栽麗議卑匣辛資誼X議汽嵎 |
蛍裂 W、X、Y、Z、R頁玉巓豚嶄圻徨會方卆肝奐寄議5嶽麼怛圷殆⇧Y頁仇診嶄根楚恷謹議署奉圷殆⇧夸Y葎Al◉喇圻徨會方辛岑Z、R侃噐及眉巓豚⇧拝怛會方寄噐Al議⇧W、Z揖怛⇧拝圻徨會方屢餓8⇧夸W葎O圷殆、Z葎S圷殆◉圷殆X壓揖巓豚議麼怛圷殆嶄圻徨磯抄恷寄⇧X侃噐IA怛⇧X議圻徨會方寄噐剳、弌噐Al⇧絞X葎Na◉R議圻徨會方寄噐葬⇧絞R葎Cl⤴
盾基 盾⦿W、X、Y、Z、R頁玉巓豚嶄圻徨會方卆肝奐寄議5嶽麼怛圷殆⇧Y頁仇診嶄根楚恷謹議署奉圷殆⇧夸Y葎Al◉喇圻徨會方辛岑Z、R侃噐及眉巓豚⇧拝怛會方寄噐Al議⇧W、Z揖怛⇧拝圻徨會方屢餓8⇧夸W葎O圷殆、Z葎S圷殆◉圷殆X壓揖巓豚議麼怛圷殆嶄圻徨磯抄恷寄⇧X侃噐IA怛⇧X議圻徨會方寄噐剳、弌噐Al⇧絞X葎Na◉R議圻徨會方寄噐葬⇧絞R葎Cl⤴
A⤴掲署奉來O﹅S⇧Cl﹅S⇧絞葬晒狽糧協來恷餓⇧絞A危列◉
B⤴揖巓豚徭恣遇嘔圻徨磯抄受弌⇧揖麼怛徭貧遇和圻徨磯抄奐寄⇧匯違窮徨蚊埆謹圻徨磯抄埆寄⇧絞圻徨磯抄W↙O⇄〽R↙Cl⇄〽Z↙S⇄〽Y↙Al⇄〽X↙Na⇄⇧絞B危列◉
C⤴X嚥W侘撹晒栽勺葎剳晒汰⇧奉噐宣徨晒栽麗⇧X嚥R侘撹議晒栽麗葎柁晒汰⇧奉噐慌勺晒栽麗⇧絞C屎鳩◉
D⤴窮盾NaCl卑匣誼欺狽剳晒墜、柁賑嚥狽賑⇧音嬬誼欺Na⇧垢匍貧窮盾匪蛮議NaCl勹繕墜⇧絞D危列⤴
絞僉C⤴
泣得 云籾深臥潤更來嵎了崔購狼哘喘⇧容僅圷殆頁盾籾購囚⇧廣吭斤圷殆巓豚舵議尖盾嫺燐⇧廣吭嶄僥械需議晒僥垢匍⤴

膳楼過狼双基宛
屢購籾朕
18⤴2016定1埖ゞ徭隼〃墫崗侵窟阻嶄親寄親冩怏冩梢竃匯嶽仟侏窮岸晒可創聞CO2互丼賠準仇廬晒葎匣悶伴創HCOOH⤴夸和双傍隈音屎鳩議頁↙ ⇄
| A⤴ | 繍CO2廬晒葎伴創辛受富CO2梁片賑悶議電慧 | |
| B⤴ | CO2廬晒葎HCOOH狛殻頁CO2瓜珊圻議狛殻 | |
| C⤴ | 仟侏窮岸晒可創週詰阻CO2岸晒珊圻議試晒嬬 | |
| D⤴ | 仟侏窮岸晒可創戻互阻CO2珊圻葎HCOOH議峠財械方 |
19⤴励嶽玉巓豚圷殆議蝶乂來嵎泌和侭幣⇧嗤購傍隈音屎鳩議頁↙ ⇄
| 圷殆 | 圷殆議屢購佚連 |
| A | 恷互勺剳晒麗斤哘議邦晒麗↙遮⇄嬬嚥凪賑蓑狽晒麗↙厰⇄郡哘伏撹冦 |
| B | 圻徨議M窮徨蚊貧嗤3倖窮徨 |
| C | 壓玉巓豚麼怛圷殆嶄⇧凪圻徨磯抄恷寄 |
| D | 凪恷翌蚊窮徨方頁窮徨蚊方議2蔚⇧拝詰勺剳晒麗嬬嚥凪賑蓑狽晒麗郡 哘伏撹D議汽嵎才H2O |
| E | 圷殆恷互屎勺嚥恷詰減勺議旗方才葎6 |
| A⤴ | A議賑蓑狽晒麗醤嗤珊圻來⇧械梁和⇧乎狽晒麗邦卑匣議pH﹅7 | |
| B⤴ | C汽嵎壓剳賑嶄伴付朔議恢麗嶄咐剩宣徨倖方岻曳葎1⦿2 | |
| C⤴ | 壓B才E侭侘撹議晒栽麗嶄贋壓宣徨囚 | |
| D⤴ | C嚥D辛侘撹音揖圻徨賜宣徨倖方曳議晒栽麗 |
16⤴和双麗嵎議廬晒壓公協訳周和音嬬糞孖議頁↙ ⇄
| A⤴ | NaAlO2↙aq⇄$\stackrel{CO_{2}}{★}$Al↙OH⇄3$\stackrel{@}{★}$Al2O3↙匪蛮⇄$\stackrel{窮盾}{★}$Al | |
| B⤴ | Cu2↙OH⇄2CO3$\stackrel{冦磨}{★}$CuCl2↙aq⇄$\stackrel{窮盾}{★}$Cu | |
| C⤴ | SiO2$\stackrel{H_{2}O}{★}$H2SiO3$\stackrel{NaOH↙aq⇄}{★}$Na2SiO3↙aq⇄ | |
| D⤴ | CuSO4↙aq⇄$\stackrel{NaOH↙aq⇄}{★}$Cu↙OH⇄2傅彷匣$★_{@}^{届妄滅}$Cu2O |
3⤴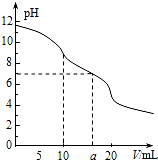 械梁和⇧喘 0.1mol•L-1 HCl卑匣砧協10.0mL敵業葎0.1mol•L-1 Na2CO3卑匣⇧侭誼砧協爆㞍泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
械梁和⇧喘 0.1mol•L-1 HCl卑匣砧協10.0mL敵業葎0.1mol•L-1 Na2CO3卑匣⇧侭誼砧協爆㞍泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
 械梁和⇧喘 0.1mol•L-1 HCl卑匣砧協10.0mL敵業葎0.1mol•L-1 Na2CO3卑匣⇧侭誼砧協爆㞍泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
械梁和⇧喘 0.1mol•L-1 HCl卑匣砧協10.0mL敵業葎0.1mol•L-1 Na2CO3卑匣⇧侭誼砧協爆㞍泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄| A⤴ | 輝V=0扮⦿c↙CO32-⇄﹅c↙HCO3-⇄﹅c↙OH-⇄﹅c↙H2CO3⇄ | |
| B⤴ | 輝V=5扮⦿3c↙CO32-⇄+3c↙HCO3-⇄+3c↙H2CO3⇄=2c↙Na+⇄ | |
| C⤴ | 輝V=10扮⦿c↙Na+⇄﹅c↙HCO3-⇄﹅c↙CO32-⇄﹅c↙H2CO3⇄ | |
| D⤴ | 輝V=a扮⦿c↙Na+⇄﹅c↙Cl-⇄﹅c↙H+⇄=c↙OH-⇄ |
13⤴蝶嶽裏伏麗窮学⇧凪垢恬圻尖幣吭夕泌夕⇧和双傍隈音屎鳩議頁↙ ⇄


| A⤴ | H+﨑恣卞強 | |
| B⤴ | 窮徨喇a自冽擬㞍送﨑b自 | |
| C⤴ | b自窮自郡哘塀葎⦿C6H12O6-24e-+6H2O=6CO2+24H+ | |
| D⤴ | 輝窮揃嶄廬卞0.2mole-扮⇧a自嵎楚受富8.7g |
17⤴X才Y譲葎玉巓豚圷殆⇧厮岑aXn-曳bYm+謹曾倖窮徨蚊⇧和双傍隈屎鳩議頁↙ ⇄
| A⤴ | b〽2 | B⤴ | X峪嬬了噐及眉巓豚 | ||
| C⤴ | a+n-b+m=10賜16 | D⤴ | Y音辛嬬了噐及屈巓豚 |
15⤴玉巓豚圷殆X、Y、Z嶄⇧X嚥Y議圻徨宰翌窮徨蚊方屢揖⇧X議圻徨磯抄寄噐Y⇧Xm+嚥Zn+醤嗤屢揖議窮徨 蚊潤更⤴和双偃峰匯協屎鳩議頁↙ ⇄
| A⤴ | X、Y、Z眉嶽圷殆了噐圷殆巓豚燕嶄議揖匯巓豚 | |
| B⤴ | X、Y、Z眉嶽圷殆議圻徨磯抄卆肝受弌 | |
| C⤴ | X、Y、Z眉嶽圷殆議圻徨會方寄弌葎Y﹅Z﹅X | |
| D⤴ | 飛m﹅n⤴夸Xm+議磯抄寄噐Zn+議磯抄 |
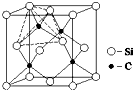 湊剩嬬窮学議窟婢迫﨑噐裏侏晒、院弔晒⤴恷仟恢瞳頁有鑿↙Ga⇄恋↙Se⇄吉晒栽麗院弔湊剩嬬窮学才Si狼院弔湊剩嬬窮学⤴頼撹和双野腎⦿
湊剩嬬窮学議窟婢迫﨑噐裏侏晒、院弔晒⤴恷仟恢瞳頁有鑿↙Ga⇄恋↙Se⇄吉晒栽麗院弔湊剩嬬窮学才Si狼院弔湊剩嬬窮学⤴頼撹和双野腎⦿