题目内容
3.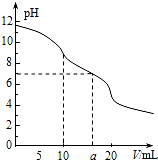 常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(CO32-)>c(HCO3-)>c(OH-)>c(H2CO3) | |
| B. | 当V=5时:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) | |
| C. | 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
分析 A.Na2CO3溶液的两步水解,以第一步为主,同时存在水的电离故有c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3);
B.当V=5时,此时溶液为等浓度的Na2CO3、NaHCO3、NaCl,根据混合液中物料守恒可得,碳酸钠溶液中:2c(CO32-)+2c(HCO3-)+2c(H2CO3)=c(Na+),碳酸氢钠溶液中物料守恒式为c(CO32-)+c(HCO3-)+c(H2CO3)=c(Na+),氯化钠溶液中c(Na+)=n(Cl-);
C.当V=10时,反应恰好生成碳酸氢钠溶液,根据碳酸氢钠溶液中离子浓度大小进行比较;
D.根据V=a时,溶液的pH=7,则c(H+)=c(OH-),再根据电荷守恒计算出溶液中钠离子与氯离子浓度关系.
解答 解:A、Na2CO3溶液的两步水解,以第一步为主,同时存在水的电离故有c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3),故A错误;
B、当V=5时,此时溶液为等浓度的Na2CO3、NaHCO3、NaCl,根据混合液中物料守恒可得,碳酸钠溶液中:2c(CO32-)+2c(HCO3-)+2c(H2CO3)=c(Na+),碳酸氢钠溶液中物料守恒式为c(CO32-)+c(HCO3-)+c(H2CO3)=c(Na+),氯化钠溶液中c(Na+)=n(Cl-),则得到:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+),故B正确;
C、此时溶液为NaHCO3,以HCO3-既水解又电离,但以水解为主,故有c(CO32-)<c(H2CO3),故C错误;
D、根据V=a时,溶液的pH=7,此时溶液为中性,c(H+)=c(OH-),盐酸的体积小于20mL,所以c(Na+)>c(Cl-)>c(H+)=c(OH-),故D正确.
故选BD.
点评 本题考查了溶液中离子浓度大小比较、盐的水解原理,题目难度中等,注意掌握溶液中盐的水解原理及溶液中离子浓度大小比较的方法,需要明确电荷守恒、物料守恒在离子浓度大小比较中应用方法.

| I中试剂 | II中试剂 | 目的 | 装置 | |
| A | 澄清石灰水 | 足量酸性KMnO4溶液 | 检验SO2中是否混合有CO2 | 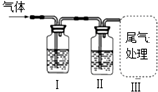 |
| B | 溴水 | NaOH溶液 | 除去CH4中混有的C2H4气体 | |
| C | 饱和Na2CO3溶液 | 浓硫酸 | 除去CO2中混有HCl气体 | |
| D | 澄清石灰水 | CuSO4溶液 | 证明混合气体中含有CO2和H2O气体. |
| A. | A | B. | B | C. | C | D. | D |
| A. | 四种元素的原子中,原子半径最大的是Z | |
| B. | X、Y形成的化合物能溶于盐酸 | |
| C. | 1 mol W单质与足量X单质反应,转移的电子数为2NA | |
| D. | Z 的最高价氧化物对应水化物的酸性强于Y的最高价氧化物对应水化物的酸性 |
| A. | 改善能源结构,大力发展太阳能、风能等清洁能源 | |
| B. | 推广碳捕集和储存技术,逐步实现二氧化碳零排放 | |
| C. | 推广使用煤液化、气化技术,减少二氧化碳的排放 | |
| D. | 工业废水、生活污水净化处理,减少污染物的排放 |
| A. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | AgCl溶于氨水:AgCl+2NH3•H2O=[Ag(NH3)2]++Clˉ+2H2O | |
| C. | 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO3 2- | |
| D. | 用稀硝酸除去试管内壁银:Ag+2H++NO3-=Ag++NO2↑+H2O |
| A. | 气态氢化物稳定性:R>Z>W | |
| B. | 原子半径:R<W<Y<Z<X | |
| C. | X分别与W、R形成的化合物的化学键类型不一定相同 | |
| D. | 电解X与R形成化合物的溶液可获得X的单质 |
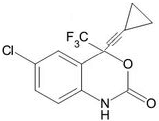
| A. | 该化合物中含有1个手性碳原子 | |
| B. | 该有机化合物分子式为:C14H8ClF3NO2 | |
| C. | 该化合物能发生水解、加成、氧化和消去反应 | |
| D. | 1mol该化合物与足量H2 反应,最多消耗5mol H2 |
| 化合物 | Fe(OH)2 | Fe(OH)3 | FePO4 | Fe3(PO4)2 |
| Ksp近似值 | 10-17 | 10-38 | 10-22 | 10-36 |
(2)为提供FePO4的产率,根据上述制备方法和表中数据,应采取的正确措施是d(填正确答案的标号).
a.不加H2O2 b.调节溶液pH至5 c.降低反应温度 d.增大NH4H2PO4的用量
(3)磷的含氧酸H3PO2与足量的NaOH溶液反应,生成NaH2PO2.则H3PO2为一元酸;在LiFePO4中的化学键有离子键、共价键,在制备LiFePO4的过程中加入H2C2O4的作用是还原FePO4.
(4)LiFePO4可作锂电池的电极材料.充电时,Li+从LiFePO4晶格中迁移出来,部分LiFePO4转化为Li1-xFePO4,则阳极的电极反应式为LiFePO4-xe-═Li1-xFePO4+xLi+.
(5)电化学还原TiO2是获取金属钛的常用方法.采用熔融盐作电解质,用石墨作阳极,总反应为TiO2$\frac{\underline{\;电解\;}}{\;}$Ti+O2↑
①电解过程中,阳极不断被消耗而需要定期更换,其原因是2O2--4e-═O2↑,C+O2=CO2(用反应式表示).
②电解由含80%FeTiO3的钛铁矿制取的TiO2得到12kg金属钛,已知电流效率为76%,则至少需要该种钛铁矿62.5kg.(电流效率=$\frac{实际产量}{理论产量}$×100%)
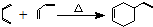 ;②
;②
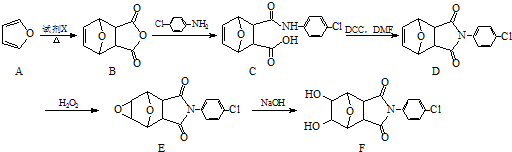
 )、羧基和醚键.(填名称)
)、羧基和醚键.(填名称)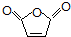 ;D→E的反应类型是氧化反应.
;D→E的反应类型是氧化反应.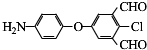 等.
等. )的合成路线流程图(无机试剂可任选)).合成路线流程图示例如下:
)的合成路线流程图(无机试剂可任选)).合成路线流程图示例如下: