题目内容
5.下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为2:1的有( )| A. | 乙酸甲酯 | B. | 对苯二酚 | C. | 2-甲基丙烷 | D. | 对苯二甲酸 |
分析 核磁共振氢谱中能出现两组峰,说明物质含有2种H原子,其峰面积之比为2:1,则两种H原子数目之比为2:1.
注意等效氢判断:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效.
解答 解:A.乙酸甲酯(CH3COOCH3)中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为1:1,故A错误;
B.对苯二酚( )中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故B正确;
)中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故B正确;
C.2-甲基丙烷中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为9:1,故C错误;
D.对苯二甲酸( )中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故D正确.
)中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故D正确.
故选:BD.
点评 本题考查有机物的结构,涉及核磁共振氢谱,关键是判断分子中H原子种类,注意等效氢判断方法,比较基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列离子方程式正确的是( )
| A. | 在三氯化铁的酸性溶液中通入足量的硫化氢:2Fe3++H2S═2Fe2++S↓+2H+ | |
| B. | PbS与CuSO4溶液反应PbS+Cu2+═CuS+Pb2+ | |
| C. | Mg(HCO3)2与过量澄清石灰水反应 Mg2++2HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O | |
| D. | 铜银合金在稀硫酸溶液中构成原电池,正极反应式 2H+2e═H2↑ |
13.油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热△H为( )
C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热△H为( )
| A. | 3.8×104kJ•mol-1 | B. | -3.8×104kJ•mol-1 | ||
| C. | 3.4×104kJ•mol-1 | D. | -3.4×104kJ•mol-1 |
4.MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
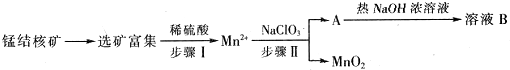
部分难溶的电解质溶度积常数(Ksp)如下表:
已知:一定条件下,MnO4-可与Mn2+反应生成MnO2
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1mol•L-1的NaClO3溶液200ml,该反应离子方程式为5Mn2++2ClO3-+4H2O=5MnO2+Cl2↑+8H+.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠.
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是MnO2+H2O+e-═MnOOH+OH-.如果维持电流强度为5A,电池工作五分钟,理论消耗锌0.5g.(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH、Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式2MnOOH+H2C2O4+2H2SO4=2CO2↑+2MnSO4+4H2O.向所得溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色沉淀成分为MnO2取少量黑色固体放入试管中,加入少量浓盐酸并加热,产生黄绿色气体,说明黑色固
体为MnO2.
(5)用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续加碱调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2,其后果和原因是Zn(OH)2、Fe(OH)2的Ksp相近,Zn2+和Fe2+分离不开.

部分难溶的电解质溶度积常数(Ksp)如下表:
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1mol•L-1的NaClO3溶液200ml,该反应离子方程式为5Mn2++2ClO3-+4H2O=5MnO2+Cl2↑+8H+.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠.
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是MnO2+H2O+e-═MnOOH+OH-.如果维持电流强度为5A,电池工作五分钟,理论消耗锌0.5g.(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH、Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式2MnOOH+H2C2O4+2H2SO4=2CO2↑+2MnSO4+4H2O.向所得溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色沉淀成分为MnO2取少量黑色固体放入试管中,加入少量浓盐酸并加热,产生黄绿色气体,说明黑色固
体为MnO2.
(5)用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续加碱调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2,其后果和原因是Zn(OH)2、Fe(OH)2的Ksp相近,Zn2+和Fe2+分离不开.
5.下列有关说法正确的是( )
| A. | pH=5的NH4Cl溶液或醋酸溶液中,由水电离出的 c(H+)均为10-9mol•L-1 | |
| B. | 常温下,将pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 | |
| C. | 在c(H+):c(OH-)=1:l012的溶液中,Na+、I-、NO3-、SO42-能大量共存 | |
| D. | 0.1 mol•L-1 Na2CO3溶液和0.1 mol•L-1 NaHSO4溶液等体积混合,溶液中:c(Na+)+c(H+)=c(CO32-)+c(SO42-)+c(HCO3-)+c(OH-) |


 ;
; ;
;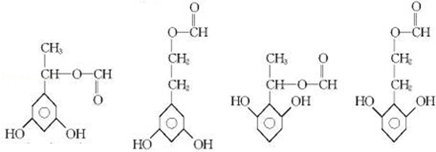 任意2种(任写两种).
任意2种(任写两种).