题目内容
15.下列离子方程式正确的是( )| A. | 在三氯化铁的酸性溶液中通入足量的硫化氢:2Fe3++H2S═2Fe2++S↓+2H+ | |
| B. | PbS与CuSO4溶液反应PbS+Cu2+═CuS+Pb2+ | |
| C. | Mg(HCO3)2与过量澄清石灰水反应 Mg2++2HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O | |
| D. | 铜银合金在稀硫酸溶液中构成原电池,正极反应式 2H+2e═H2↑ |
分析 A.硫化氢显酸性,并且硫有还原性,三价铁具有氧化性,两者反应生成硫单质和亚铁离子,该离子方程式电荷、原子守恒;
B.难溶电解质的溶解平衡及沉淀转化是溶解度大的物质向溶解度小的物质转化,沉淀溶解平衡的转化需用可逆符号;
C. Mg(HCO3)2与过量澄清石灰水反应,生成氢氧化镁和碳酸钙沉淀;
D.铜银合金在稀硫酸溶液中构成原电池,氧气在正极上放电,以吸氧腐蚀为主,负极铜失去电子.
解答 解:A.在三氯化铁的酸性溶液中通入足量的硫化氢会发生氧化还原反应:2Fe3++H2S═2Fe2++S↓+2H+,故A正确;
B.沉淀向溶解度更小的方向转化,PbS与CuSO4溶液反应PbS+Cu2+?CuS+Pb2+,故B错误;
C.氢氧化镁的溶解度小于碳酸镁,所以Mg(HCO3)2与过量澄清石灰水反应生成氢氧化镁和碳酸钙沉淀,离子反应为:Mg2++2HCO3-+Ca2++4OH-═Mg(OH)2↓+CaCO3↓+CO32-++2H2O,故C错误;
D.铜银合金在稀硫酸溶液中构成原电池,氧气在正极上放电,电极反应为:O2+4e-+4H+=2H2O,故D错误;
故选A.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,该题还需注意反应的原理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列有关实验操作、现象、解释和结论都正确的是( )
| 选项 | 操 作 | 现 象 | 解释、结论 |
| A | 用玻璃棒蘸取浓氨水点到干燥红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | 向蔗糖中加入浓硫酸并搅拌 | 蔗糖变黑,体积膨胀 | 反应中浓硫酸只体现脱水性 |
| D | 过量的Fe粉与氯气充分反应后,向反应后的混合物中加水,取上层清液滴入KSCN溶液 | 溶液不变红色 | 氯气将Fe氧化为Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
3.短周期元素X、Y、Z、W的原子序数依次增大,X、Y、Z同主族,W的氧化物是形成酸雨的主要原因之一.下列说法正确的是( )
| A. | Y的单质在氧气中燃烧生成Y2O | |
| B. | X、W的简单离子均能促进水的电离 | |
| C. | 原子半径由小到大的顺序为X<Y<Z<W | |
| D. | Z单质加入到Y的可溶性盐溶液中,可以置换出Y |
10.下列说法正确的是( )
| A. | 钢化玻璃的成分与普通玻璃一样,有机玻璃是聚合物 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苹和甲苯互为同系物,均能使KMnCL4酸性溶液褪色 | |
| D. | 按系统命名法,化合物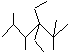 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
20.化学与生产、生活 密切相关,背景材料:
①北大研制的石墨烯弹性气凝胶(又名碳海棉)入选2013年度世界最轻固体材料;
②2014年11月上旬北京APEC峰会期间,政府重拳整治雾霾,蓝天重现;
③用铂丝或无锈铁丝可用来进行钠、钾、铜、钡、锶等的焰色反应
④瑞典皇家理工学院(KTH)的研究人员已经成功地构建出了一种能使水快速分解的分子催化剂.
下列说法不正确的是( )
①北大研制的石墨烯弹性气凝胶(又名碳海棉)入选2013年度世界最轻固体材料;
②2014年11月上旬北京APEC峰会期间,政府重拳整治雾霾,蓝天重现;
③用铂丝或无锈铁丝可用来进行钠、钾、铜、钡、锶等的焰色反应
④瑞典皇家理工学院(KTH)的研究人员已经成功地构建出了一种能使水快速分解的分子催化剂.
下列说法不正确的是( )
| A. | 石墨烯弹性气凝胶可用作处理海上原油泄漏的吸油材料 | |
| B. | 压减燃煤、严格控车、调整产业是治理雾霾有效措施 | |
| C. | 绚丽缤纷彩色的烟花中添加了含钾、钠、铁、铜等金属化合物 | |
| D. | 使用该分子催化剂可将一次能源太阳能直接转化成二次能源,例如电能、氢能 |
7.化学与我们的生活息息相关.下列说法不正确的是( )
| A. | 玻璃、水晶和陶瓷都是传统硅酸盐材料 | |
| B. | 可溶性铝盐和铁盐可用作净水剂 | |
| C. | SO2和NO都能形成酸雨而破坏环境 | |
| D. | CO2和CH4都是引起温室效应的气体 |
4.下列关于有机物的说法错误的是( )
| A. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| B. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| C. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| D. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 |
5.下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为2:1的有( )
| A. | 乙酸甲酯 | B. | 对苯二酚 | C. | 2-甲基丙烷 | D. | 对苯二甲酸 |

 ,写出该反应的化学方程式
,写出该反应的化学方程式 .
. )在POCl3(三氯氧磷)的催化下反应生成E,同时还生成H2O和另一种有机物,写出该有机物的分子式C2H7N.
)在POCl3(三氯氧磷)的催化下反应生成E,同时还生成H2O和另一种有机物,写出该有机物的分子式C2H7N. 或
或 .(写出其中一种的结构简式)
.(写出其中一种的结构简式) 和(CH3CO)2O为原料制备
和(CH3CO)2O为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: