题目内容
工业合成有机物F路线如下:

(1)有机物E中含氧的官能团名称为 和
(2)化合物D的结构简式是
(3)在上述转化关系中,设计步骤(b)和(d)的
(4)写出步骤(e)的化学反应方程式
(5)写出同时满足下列条件的C的一种同分异构体的结构简式
A.属于芳香化合物B.核磁共振谱有四个峰C.1mol该物质最多可以消耗1molNa
(6)已知①RCH=CH2+HBr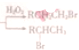 (R:烃基或氧原子,R′:烃基)
(R:烃基或氧原子,R′:烃基)
②RCHO+
RCH= 写出以丙烯和
写出以丙烯和 为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
CH3CHO
CH3COOH.

(1)有机物E中含氧的官能团名称为
(2)化合物D的结构简式是
(3)在上述转化关系中,设计步骤(b)和(d)的
(4)写出步骤(e)的化学反应方程式
(5)写出同时满足下列条件的C的一种同分异构体的结构简式
A.属于芳香化合物B.核磁共振谱有四个峰C.1mol该物质最多可以消耗1molNa
(6)已知①RCH=CH2+HBr
 (R:烃基或氧原子,R′:烃基)
(R:烃基或氧原子,R′:烃基)②RCHO+

| OH- |
| -H2O |
 写出以丙烯和
写出以丙烯和 为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2| O2 |
| 催化剂 |
| O2 |
| 催化剂 |
考点:有机物的合成
专题:
分析:(1)根据有机物E的结构简式可判断官能团;
(2)题中流程图可知D的结构简式;
(3)b到d反应前后不变的为-OH,过程中发生氧化反应,则肯定为保护羟基不被氧化;
(4)步骤e 的反应为消去反应;
(5)A.属于芳香化合物,应含有苯环;B.核磁共振氢谱有四个峰,说明四种性质不同的H;C.1mol该物质最多可以消耗1molNa,应含有一个-OH,结合C的结构可以判断;
(6)以丙烯和 为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与
为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与 发生信息中的反应即可得A.
发生信息中的反应即可得A.
(2)题中流程图可知D的结构简式;
(3)b到d反应前后不变的为-OH,过程中发生氧化反应,则肯定为保护羟基不被氧化;
(4)步骤e 的反应为消去反应;
(5)A.属于芳香化合物,应含有苯环;B.核磁共振氢谱有四个峰,说明四种性质不同的H;C.1mol该物质最多可以消耗1molNa,应含有一个-OH,结合C的结构可以判断;
(6)以丙烯和
 为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与
为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与 发生信息中的反应即可得A.
发生信息中的反应即可得A.解答:
解:(1)分析有机物E的结构简式可知有机物D中含氧的官能团名称为羰基、酯基,故答案为:羰基;羟基;
(2)根据题中流程图可知D的结构简式为 ,故答案为:
,故答案为: ;
;
(3)b到d反应前后不变的为-OH,过程中发生氧化反应,则肯定为保护羟基不被氧化,故答案为:保护醇-OH;
(4)对比E和F的分子式结合反应条件可知E生成F的反应为消去反应,则F应为 ,所以步骤e 的反应方程式为
,所以步骤e 的反应方程式为
 +H2O,
+H2O,
故答案为:
 +H2O;
+H2O;
(5)A.属于芳香化合物,应含有苯环;B.核磁共振氢谱有四个峰,说明四种性质不同的H;C.1mol该物质最多可以消耗1molNa,应含有一个-OH,则符合条件的C的同分异构体为 ,
,
故答案为: ;
;
(6)以丙烯和 为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与
为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与 发生信息中的反应即可得A,反应的流程为
发生信息中的反应即可得A,反应的流程为 ,
,
故答案为: .
.
(2)根据题中流程图可知D的结构简式为
 ,故答案为:
,故答案为: ;
;(3)b到d反应前后不变的为-OH,过程中发生氧化反应,则肯定为保护羟基不被氧化,故答案为:保护醇-OH;
(4)对比E和F的分子式结合反应条件可知E生成F的反应为消去反应,则F应为
 ,所以步骤e 的反应方程式为
,所以步骤e 的反应方程式为
| 浓H2SO4 |
| △ |
 +H2O,
+H2O,故答案为:

| 浓H2SO4 |
| △ |
 +H2O;
+H2O;(5)A.属于芳香化合物,应含有苯环;B.核磁共振氢谱有四个峰,说明四种性质不同的H;C.1mol该物质最多可以消耗1molNa,应含有一个-OH,则符合条件的C的同分异构体为
 ,
,故答案为:
 ;
;(6)以丙烯和
 为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与
为原料制备A物质,可以先将丙烯与溴化氢加成再水解、氧化得到丙酮,丙酮与 发生信息中的反应即可得A,反应的流程为
发生信息中的反应即可得A,反应的流程为 ,
,故答案为:
 .
.
点评:本题考查有机物的合成,题目难度中等,综合考查有机物的结构和性质,解答的关键是把握题给信息,根据有机物官能团的变化判断有机物的反应类型,书写相关反应的化学方程式,易错点为(6),注意结合题意可逆向推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
航天飞机用的铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4
N2↑+4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
| ||
| A、反应属于分解反应 |
| B、上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C、反应从能量变化上说,主要是化学能转变为热能和动能 |
| D、在反应中高氯酸铵只起氧化剂作用 |
下列离子方程式书写不正确的是( )
| A、向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | ||||
| B、碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | ||||
| C、向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
D、铁棒作阴极,碳棒作阳极电解饱和氯化钠溶液:2Cl _+2H2O
|
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法不正确的是( )
| A、化合物BmAm分子中所有原子一定共平面 |
| B、一定条件下,元素C、D、E的最高价氧化物对应的水化物之间能发生反应 |
| C、工业上常用电解法制备元素C、D、E的单质 |
| D、化合物BAn与BEn具有相同类型的化学键 |

 某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:
某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:


 :
: