题目内容
下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题

(1)表中M的元素符号是 ,A元素的最高价氧化物的化学式为 ;
(2)B和D的氢化物稳定性 > (填化学式)
(3)写出C和E形成化合物的电子式: .

(1)表中M的元素符号是
(2)B和D的氢化物稳定性
(3)写出C和E形成化合物的电子式:
考点:元素周期律和元素周期表的综合应用
专题:
分析:根据元素在周期表中的位置可以确定元素种类,依据元素周期律中原子半径和金属性强弱的判定作答.
(1)M位于第三周期第IVA族,是硅元素,A是碳元素,据此解答即可;
(2)根据元素的非金属性越强,其气态氢化物越稳定;
(3)根据元素在周期表中的位置可以确定C和E分别为Na、Cl,形成的化合物是离子化合物NaCl,据此解答即可.
(1)M位于第三周期第IVA族,是硅元素,A是碳元素,据此解答即可;
(2)根据元素的非金属性越强,其气态氢化物越稳定;
(3)根据元素在周期表中的位置可以确定C和E分别为Na、Cl,形成的化合物是离子化合物NaCl,据此解答即可.
解答:
解:(1)M位于第三周期第IVA族,是硅元素,元素符号为Si,A是碳元素,碳的最高价氧化物为二氧化碳,化学式为:CO2,
故答案为:Si;CO2;
(2)元素的非金属性越强,其气态氢化物越稳定,由于同一主族中,非金属性随着原子序数增大而减小,故非金属性O>S,故氢化物的稳定性:H2O>H2S,
故答案为:H2O、H2S;
(3)C和E分别为Na、Cl,分别属于活泼金属与活泼非金属,形成的化合物是离子化合物NaCl,电子式为: 故答案为:
故答案为: .
.
故答案为:Si;CO2;
(2)元素的非金属性越强,其气态氢化物越稳定,由于同一主族中,非金属性随着原子序数增大而减小,故非金属性O>S,故氢化物的稳定性:H2O>H2S,
故答案为:H2O、H2S;
(3)C和E分别为Na、Cl,分别属于活泼金属与活泼非金属,形成的化合物是离子化合物NaCl,电子式为:
 故答案为:
故答案为: .
.
点评:本题主要考查元素周期表的结构和元素周期律综合应用,通过元素在周期表中的位置确定是何种元素是解题的关键,试题比较基础,难度中等.

练习册系列答案
相关题目
如果浓苯酚溶液溅到皮肤上,最好采用的洗涤液是( )
| A、用水冲洗 |
| B、用NaOH溶液洗 |
| C、用苯洗 |
| D、用酒精清洗 |

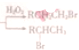 (R:烃基或氧原子,R′:烃基)
(R:烃基或氧原子,R′:烃基)
 写出以丙烯和
写出以丙烯和 为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2



 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基)