题目内容
下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ,⑥ ,⑦ ,? .
(2)在这些元素中,最活泼的金属元素是 最活泼的非金属元素是 ,电负性最大的是 .
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 (只写一种),写出三者之间相互反应的离子方程式 .
(4)在这些元素中,原子半径最小的是 ,原子半径最大的是 ,第一电离能最小的是 .
(5)在③与④中,化学性质较活泼的是 ,怎样用化学实验证明?答: .
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | ① | ② | ? | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ? | ? |
(2)在这些元素中,最活泼的金属元素是
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(4)在这些元素中,原子半径最小的是
(5)在③与④中,化学性质较活泼的是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:(1)由元素在周期表中位置,可知①为N、②为O、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为P、⑧为S、⑨为Cl、⑩为K、?为Ca、?为Se、?为F;
(2)同周期自左而右金属性减弱、非金属性增强、元素电负性增大,同主族自上而下金属性增强、非金属性减弱、元素电负性减小;
(3)最高价含氧酸最强的为高氯酸;K的金属性最强,故氢氧化钾碱性最强;氢氧化铝属于两性氢氧化物;
(4)同周期自左而右原子半径减小、同主族自上而下原子半径增大;金属性越强、第一电离能越小;
(5)金属性越强越活泼,用它们跟水反应的实验证明.
(2)同周期自左而右金属性减弱、非金属性增强、元素电负性增大,同主族自上而下金属性增强、非金属性减弱、元素电负性减小;
(3)最高价含氧酸最强的为高氯酸;K的金属性最强,故氢氧化钾碱性最强;氢氧化铝属于两性氢氧化物;
(4)同周期自左而右原子半径减小、同主族自上而下原子半径增大;金属性越强、第一电离能越小;
(5)金属性越强越活泼,用它们跟水反应的实验证明.
解答:
解:(1)由元素在周期表中位置,可知①为N、②为O、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为P、⑧为S、⑨为Cl、⑩为K、?为Ca、?为Se、?为F,
故答案为:N;Si;N;Ca;
(2)同周期自左而右金属性减弱、非金属性增强、元素电负性增大,同主族自上而下金属性增强、非金属性减弱、元素电负性减小,故上述元素中K的金属性最强、F元素非金属性最强、F的电负性最大,
故答案为:K;F;F;
(3)F元素的非金属性最强,但F元素没有最高价氧化物的水化物,最高价氧化物的水化物酸性最强的是HClO4,上述元素中K的金属性最强,故KOH的碱性最强,Al(OH)3是两性氢氧化物,三种物质两两之间离子反应方程式为分别为:H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:HClO4;KOH;Al(OH)3;H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O;
(4)同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径最小的是F,原子半径最大的是K,K的金属性最强,故K的第一电离能最小,
故答案为:F;K;K;
(5)Na的金属性比Mg强,故Na更活泼,可以用它们跟水反应的实验证明:钠跟水剧烈反应,放出氢气,并生成强碱,Mg跟沸水才反应,并生成中强碱,
故答案为:Na;可以用它们跟水反应的实验证明:钠跟水剧烈反应,放出氢气,并生成强碱,Mg跟沸水才反应,并生成中强碱.
故答案为:N;Si;N;Ca;
(2)同周期自左而右金属性减弱、非金属性增强、元素电负性增大,同主族自上而下金属性增强、非金属性减弱、元素电负性减小,故上述元素中K的金属性最强、F元素非金属性最强、F的电负性最大,
故答案为:K;F;F;
(3)F元素的非金属性最强,但F元素没有最高价氧化物的水化物,最高价氧化物的水化物酸性最强的是HClO4,上述元素中K的金属性最强,故KOH的碱性最强,Al(OH)3是两性氢氧化物,三种物质两两之间离子反应方程式为分别为:H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:HClO4;KOH;Al(OH)3;H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O;
(4)同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径最小的是F,原子半径最大的是K,K的金属性最强,故K的第一电离能最小,
故答案为:F;K;K;
(5)Na的金属性比Mg强,故Na更活泼,可以用它们跟水反应的实验证明:钠跟水剧烈反应,放出氢气,并生成强碱,Mg跟沸水才反应,并生成中强碱,
故答案为:Na;可以用它们跟水反应的实验证明:钠跟水剧烈反应,放出氢气,并生成强碱,Mg跟沸水才反应,并生成中强碱.
点评:本题考查元素周期表与元素周期律,解答本题的关键是掌握:1~20号元素的名称及符号,元素周期表的结构,能根据元素周期表中元素性质的递变规律进行分析判断,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列化学用语或模型表示正确的是( )
| A、乙烯的结构简式为CH2CH2 |
B、羟基的电子式: |
C、Mg2+结构示意图: |
D、C2H4分子比例模型: |
下列物质属于共价化合物的是( )
| A、O2 |
| B、Na2O |
| C、HCl |
| D、NH4Cl |
下列离子方程式正确的是( )
| A、Fe(OH)3与氢硫酸溶液混合:Fe(OH)3+3 H+═Fe3++3H2O |
| B、1mol?L-1的NaAlO2溶液和2.5mol?L-1的HCl等体积互相均匀混合:2AlO2-+5H+═Al(OH)3↓+Al3++H2O |
| C、向硫酸铝按[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-═AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| D、碳酸氢镁溶液中加入足量氢氧化钠:Mg2++2HCO3-+2OH-═MgCO3↓+2H2O+CO2↑ |
下列说法中正确的是( )
| A、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| B、淀粉、纤维素、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
| C、只用水就能鉴别苯、乙醇和四氯化碳 |
| D、分子式C4H8Cl2的有机物,分子中含2个甲基的同分异构体有3种 |

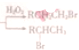 (R:烃基或氧原子,R′:烃基)
(R:烃基或氧原子,R′:烃基)
 写出以丙烯和
写出以丙烯和 为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2