题目内容
X、Y和z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同.回答下列问题:
(1)z元素位于周期表第 周期,第 族.z单质与水反应的离子方程式为
(2)由、X、Y、z三种元素组成的化合物中,含有的化学键类型有 (填字母)
A.离子键 B.极性共价键 C.非极性共价键
(3)x和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是 (填化学式),此化合物可将碱性工业废水中的cN氧化为碳酸盐和氨,相应的离子方程式为 .
(1)z元素位于周期表第
(2)由、X、Y、z三种元素组成的化合物中,含有的化学键类型有
A.离子键 B.极性共价键 C.非极性共价键
(3)x和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,则X是H元素;Y原子最外层电子数是其周期数的三倍,最外层电子数不超过8个,第一电子层为最外层不超过2个,则Y是O元素;Z与X原子最外层电子数相同,且原子序数大于Y,则Z为Na元素,据此结合元素周期律知识进行解答.
解答:
解:X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,则X是H元素;Y原子最外层电子数是其周期数的三倍,最外层电子数不超过8个,第一电子层为最外层不超过2个,则Y是O元素;Z与X原子最外层电子数相同,且原子序数大于Y,则Z为Na元素,
(1)根据上面的分析可知,Z为Na元素,位于周期表中第三周期、ⅠA族;钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:三;ⅠA;2Na+2H2O=2Na++2OH-+H2↑;
(2)由H、O、Na三种元素组成的化合物为NaOH,氢氧化钠为离子化合物,NaOH既含有离子键,也含有极性共价键,则AB正确,
故答案为:AB;
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质是过氧化氢,过氧化氢还可将碱性工业废水中的CN-氧化为碳酸盐和氨,方程式为:H2O2+CN-+OH-=CO32-+NH3,
故答案为:H2O2;H2O2+CN-+OH-=CO32-+NH3.
(1)根据上面的分析可知,Z为Na元素,位于周期表中第三周期、ⅠA族;钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:三;ⅠA;2Na+2H2O=2Na++2OH-+H2↑;
(2)由H、O、Na三种元素组成的化合物为NaOH,氢氧化钠为离子化合物,NaOH既含有离子键,也含有极性共价键,则AB正确,
故答案为:AB;
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质是过氧化氢,过氧化氢还可将碱性工业废水中的CN-氧化为碳酸盐和氨,方程式为:H2O2+CN-+OH-=CO32-+NH3,
故答案为:H2O2;H2O2+CN-+OH-=CO32-+NH3.
点评:本题考查了元素位置、结构与性质的应用,题目难度中等,熟悉元素周期表结构、元素周期律内容为解本题关键,注意熟练掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| B、淀粉、纤维素、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
| C、只用水就能鉴别苯、乙醇和四氯化碳 |
| D、分子式C4H8Cl2的有机物,分子中含2个甲基的同分异构体有3种 |

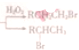 (R:烃基或氧原子,R′:烃基)
(R:烃基或氧原子,R′:烃基)
 写出以丙烯和
写出以丙烯和 为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
为原料制备A物质的合成路线图(无机试剂任选),合成路线流程图如下:CH2=CH2
