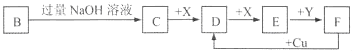题目内容
香叶醛分子的结构简式如图所示.下列叙述正确的是( )
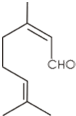

| A、1 mol香叶醛发生加成反应需要2 mol H2 |
| B、香叶醛不能与溴发生反应 |
| C、香叶醛能与钠发生反应生成H2 |
| D、香叶醛能发生银镜反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:分子中含有碳碳双键,可发生加成、加聚和氧化反应,含有醛基,可发生加成和氧化反应,以此解答该题.
解答:
解:A.分子中的碳碳双键和醛基都可与氢气发生加成反应,则1 mol香叶醛发生加成反应需要3 mol H2,故A错误;
B.含有碳碳双键,可与溴发生加成反应,且醛基可被溴氧化,故B错误;
C.分子中不含羟基,不能与钠反应,故C错误;
D.含有醛基,可发生银镜反应,故D正确.
故选D.
B.含有碳碳双键,可与溴发生加成反应,且醛基可被溴氧化,故B错误;
C.分子中不含羟基,不能与钠反应,故C错误;
D.含有醛基,可发生银镜反应,故D正确.
故选D.
点评:本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,明确结构决定物质的性质,熟悉物质中的官能团及常见物质的性质即可解答,难度不大.

练习册系列答案
相关题目
NA表示阿佛加德罗常数,下列说法正确的是( )
| A、60克SiO2含有2NA个Si-O共价键 |
| B、1.0L 1.0mo1/L的NaAlO2水溶液中含有的氧原子数为2NA |
| C、8.2g Na218O2与足量的CO2和H2O(g)的混合气体充分反应后转移电子数为0.1NA |
| D、NA个Fe(OH)3胶体粒子的质量为107g |
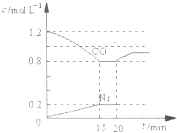
达平衡状态的可逆反应:N2(g)+3H2(g)?2NH3(g),改变某一条件,一段时间后,测得正反应速率以N2的浓度减小表示:v(N2)=0.6mol/(L?min),逆反应速率以NH3的浓度减小表示:v(NH3)=1.2mol/(L?min),此时可逆反应的状态是( )
| A、测定时,v正>v逆 |
| B、测定时,v正<v逆 |
| C、测定时,v正=v逆 |
| D、不可能达到新平衡 |
在水中存在H2O?H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡发生移动( )
| A、加入NaOH固体 |
| B、加入NaCl固体 |
| C、加入CH3COOH固体 |
| D、升温 |
25℃时,水的电离达到平衡;H2O?H-+OH-△H>0,下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、向水中加入少量固体硫酸氢钠,c(H-)降低 |
| C、向水中加入少量固体氢氧化钠,平衡正向移动,c(H-)降低 |
| D、将水加热,KW增大,pH不变 |
将一定量的锌与100mL 18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成16.8L气体(标准状况),将反应后的溶液稀释到1L,测得溶液的c(H+)=1mol/L,则下列叙述中错误的是( )
| A、气体A为二氧化硫和氢气的混合物 |
| B、气体A中二氧化硫和氢气的体积比为4:1 |
| C、反应中共消耗锌95.5g |
| D、反应中共转移电子1.5mol |
对于同一周期从左到右的主族元素,下列说法中正确的是( )
| A、原子半径逐渐减小 |
| B、元素的金属性逐渐增强 |
| C、最高正化合价逐渐增大 |
| D、单质的熔沸点逐渐降低 |

 已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);
已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);