题目内容
11.下列各组顺序的排列不正确的是 ( )| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H2SO4 | D. | 热稳定性H2O>H2Se>H2S |
分析 A、根据同周期原子半径的递变规律:同周期元素原子的半径从左到右依次减小解答;
B、根据同周期气态氢化物的递变规律:从左到右逐渐增强可以判断;
C、根据同周期、同主族最高价含氧酸的递变规律可以得出正确判断;
D、原子的得电子能力越强,氢化物的稳定性越强,据此回答.
解答 解:A.同周期元素原子的半径从左到右依次减小,则原子半径:Al<Mg<Na,故A错误;
B.同周期元素气态氢化物的稳定性从左到右逐渐增强,即热稳定性:HCl>H2S>PH3,故B正确;
C.同周期最高价氧化物对应水合物的酸性从左到右依次增强(Si、P同周期),同主族最高价氧化物对应水合物的酸性从上到下依次减弱(C、Si同主族),
则酸性强弱:H2SiO4<H2CO3<H2SO4,故C正确;
D、原子的得电子能力顺序:O>S>Se,所以热稳定性H2O>H2Se>H2S,故D正确.
故选A.
点评 本题考查的主要是同周期元素性质的递变规律,运用递变规律解题要判断是同周期还是同主族,才能正确运用规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.某同学按下述操作配制100 mL 0.20 mol•L-1Na2SO4溶液,请回答有关问题.
(2)取出该Na2SO4溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是0.04mol/L.
(3)在实验中,以下操作对实验结果没有影响的是C.
A.没有将洗涤液转移到容量瓶中
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
(4)请写出检验溶液中的SO42-的具体操作:取少量待测液,滴加稀盐酸,若无明显现象,再滴加氯化钡溶液,产生白色沉淀.
| (1)实验步骤 | 有关问题 |
| ①计算所需Na2SO4的质量 | 需要称量Na2SO4的质量为2.8g |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是:托盘天平 |
| ③将Na2SO4加入100mL烧杯中,并加入适量水 | 用玻璃棒搅拌至完全溶解,冷却至室温 |
| ④将烧杯中溶液转移至仪器A中(已检查不漏水) | 仪器A是100mL容量瓶; |
| ⑤洗涤烧杯,转移,定容 | |
| ⑥摇匀、装瓶、贴上标签 |
(3)在实验中,以下操作对实验结果没有影响的是C.
A.没有将洗涤液转移到容量瓶中
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
(4)请写出检验溶液中的SO42-的具体操作:取少量待测液,滴加稀盐酸,若无明显现象,再滴加氯化钡溶液,产生白色沉淀.
1.研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,其放电工作原理如图所示.下列说法正确的是( )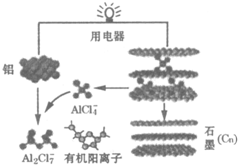

| A. | 放电时,有机阳离子向铝电极方向移动 | |
| B. | 充电时,铝电极连接外加电源的正极,石墨电极连接外加电源的负极 | |
| C. | 放电时负极的电极反应为:Al-3e-+7AlCl4-=4Al2Cl7- | |
| D. | 该电池的工作原理为:3Cn+4Al2Cl7-$?_{充电}^{放电}$3CnAlCl4+Al+AlCl4- |