题目内容
3.完成下列反应离子方程式①在液氨中投入一小块金属钠,放出气体2Na+2NH3=H2↑+2NaNH2.
②NaNH2溶于水的反应NH2-+H2O=OH-+NH3↑.
③类似于“H++OH-=H2O”的反应NH2-+NH4+=2NH3↑.
分析 ①在液氨中投入一小块金属钠,反应生成氢气和NaNH2;
②NaNH2溶于水生成氢氧化钠和氨气,据此写出反应的离子方程式;
③类比“H++OH-=H2O”可知,NH2-与NH4+发生反应生成NH3.
解答 解:①在液氨中投入一小块金属钠,放出气体,气体为氢气,反应的化学方程式为:2Na+2NH3=H2↑+2NaNH2,
故答案为:2Na+2NH3=H2↑+2NaNH2;
②NaNH2溶于水生成氢氧化钠和氨气,反应的离子方程式为:NH2-+H2O=OH-+NH3↑,
故答案为:NH2-+H2O=OH-+NH3↑;
③类比“H++OH-=H2O”可知,NH2-与NH4+发生反应生成NH3,反应的离子方程式为:NH2-+NH4+=2NH3↑,
故答案为:NH2-+NH4+=2NH3↑.
点评 本题考查了离子方程式的书写,为高考的高频题,题目难度中等,明确离子方程式的书写原则为解答关键,试题侧重考查了学生的知识迁移能力.

练习册系列答案
相关题目
13.常温下时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)同浓度的醋酸钠、次氯酸钠、碳酸钠三种溶液的pH值由小到大的顺序为Na2CO3>NaClO>CH3COONa.
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)同浓度的醋酸钠、次氯酸钠、碳酸钠三种溶液的pH值由小到大的顺序为Na2CO3>NaClO>CH3COONa.
11.下列各组顺序的排列不正确的是 ( )
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H2SO4 | D. | 热稳定性H2O>H2Se>H2S |
18.下列氯元素含氧酸酸性最强的是( )
| A. | HClO | B. | HClO2 | C. | HClO3 | D. | HClO4 |
8.几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )
| 元素代号 | 原子半径/nm | 主要化合价 |
| X | 0.160 | +2 |
| Y | 0.143 | +3 |
| Z | 0.102 | +6、-2 |
| L | 0.099 | +7、-1 |
| M | 0.077 | +4、-4 |
| Q | 0.074 | -2 |
| A. | Z的氢化物的稳定性强于L的氢化物的稳定性 | |
| B. | Y与Q形成的化合物不能跟氢氧化钠溶液反应 | |
| C. | 等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多 | |
| D. | 在化学反应中,M原子与其他原子易形成共价键而不易形成离子键 |
15.下列除杂的方法错误的是( )
| 物质 | 杂质 | 除杂试剂 | 主要操作 | |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | Mg | Al | NaOH溶液 | 过滤 |
| C | FeCl2 | FeCl3 | Cu | 过滤 |
| D | NaCl | 泥沙 | 加水 | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
13.标况下,某混合气体由两种气态烃组成,2.24L该混合气体完全燃烧后,得到4.48L二氧化碳和3.6克水,则这两种气体可能是( )
| A. | CH4和 C3H8 | B. | CH4和C3H4 | C. | C2H2和C3H4 | D. | C2H4和C2H6 |
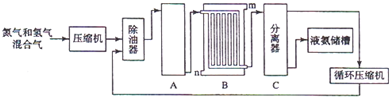
 H2+CO,CH4+H2O
H2+CO,CH4+H2O 3H2+CO;
3H2+CO; ;
;