题目内容
1.研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,其放电工作原理如图所示.下列说法正确的是( )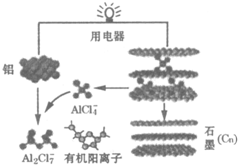
| A. | 放电时,有机阳离子向铝电极方向移动 | |
| B. | 充电时,铝电极连接外加电源的正极,石墨电极连接外加电源的负极 | |
| C. | 放电时负极的电极反应为:Al-3e-+7AlCl4-=4Al2Cl7- | |
| D. | 该电池的工作原理为:3Cn+4Al2Cl7-$?_{充电}^{放电}$3CnAlCl4+Al+AlCl4- |
分析 放电时,活泼的金属铝是负极,放电时负极发生氧化反应生成铝离子,铝离子与AlCl4-结合生成Al2Cl7-;不活泼石墨为正极,原电池中阳离子向正极移动,在二次电池充电时,电源的正极和原电池的正极相连,原电池的负极和电源的负极相连.
解答 解:A、放电时,活泼的金属铝是负极,不活泼石墨为正极,放电时,有机阳离子向正极石墨电极方向移动,故A错误;
B、电时,铝电极连接外加电源的负极,石墨电极连接外加电源的正极,故B错误;
C、放电时,活泼的金属铝是负极,电极反应为:Al-3e-+7AlCl4-=4Al2Cl7-,故C正确;
D、放电时负极发生氧化反应生成铝离子,铝离子与AlCl4-结合生成Al2Cl7-,所以电极反应式为:Al-3e-+7AlCl4-═4Al2Cl7-,正极上电极反应式为:CnAlCl4+e-═Cn+AlCl4-,两极反应相加得到总反应:3CnAlCl4+Al+4AlCl4-$?_{充电}^{放电}$4Al2Cl7-+3Cn,故D错误.
故选C.
点评 本题考查学生二次电池的工作原理以及原电池和电解池的工作原理知识,属于综合知识的考查,难度中等.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
11.下列各组顺序的排列不正确的是 ( )
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H2SO4 | D. | 热稳定性H2O>H2Se>H2S |
9.用下列实验装置进行相应实验,能达到实验目的是( )
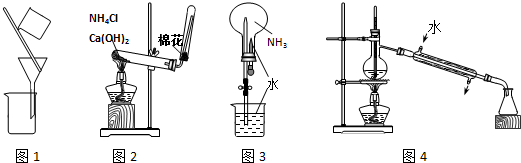

| A. | 用图1装置分离乙醇和乙酸 | B. | 用图2装置制取氨气 | ||
| C. | 用图3装置进行氨气的喷泉实验 | D. | 用图4装置进行石油的分馏实验 |
16.下列说法中,正确的是( )
| A. | 苯和甲苯都能与卤素单质、硝酸等发生取代反应 | |
| B. | 苯的同系物是分子中仅含有一个苯环的所有烃类物质 | |
| C. | 烯烃在适宜的条件下只能发生加成反应不能发生取代反应 | |
| D. | 分子式是C4H8的烃分子中一定含有碳碳双键 |
6.判断下列元素中不属于主族元素的是( )
| A. | 钡 | B. | 铅 | C. | 碘 | D. | 铁 |
13.标况下,某混合气体由两种气态烃组成,2.24L该混合气体完全燃烧后,得到4.48L二氧化碳和3.6克水,则这两种气体可能是( )
| A. | CH4和 C3H8 | B. | CH4和C3H4 | C. | C2H2和C3H4 | D. | C2H4和C2H6 |
10.下列有关叙述中正确的是( )
| A. | 溶液中大量共存:Na+、Ba2+、Cl-、CO32- | |
| B. | 无色溶液中能大量共存:NH4+、Fe3+、SO42-、CI- | |
| C. | 氢氧化铁跟硫酸反应的离子方程式是:3H++Fe(OH)3═Fe3++3H2O | |
| D. | 碳酸氢钠溶液跟氢氧化钠反应的离子方程式是:HCO3-+OH-═H2O+CO2↑ |
11.在一定条件下,将A和B各0.32mol充入10L的恒容密闭容器中,发生如下反应:A(g)+B(g)═2C(g)△H<0.反应过程中测定的数据如下表,下列说法正确的是( )
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 其他条件不变,向平衡体系中再充入0.32molA,再达到新平衡时,B的转化率增大 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,起始时向容器中充入0.64molA和B,平衡时,n(C)<0.48mol | |
| D. | 反应前2min的平均速率ν(C)=0.004mol•(L•min)-1 |