13��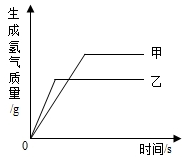 �мס������ֽ������������������ϡ�����У����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�������н��ۺ������ǣ�������
�мס������ֽ������������������ϡ�����У����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�������н��ۺ������ǣ�������
 �мס������ֽ������������������ϡ�����У����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�������н��ۺ������ǣ�������
�мס������ֽ������������������ϡ�����У����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�������н��ۺ������ǣ�������| A�� | ������Լף��� | B�� | ���������������ף��� | ||
| C�� | ���뷴Ӧ�����������ף��� | D�� | ���뷴Ӧ�Ľ��������ף��� |
10����ѧ��ȤС���ͬѧ���������ʵļ���չ�������ۣ����в���ȷ���ǣ�������
| A�� | ����CO2�����������NaOH��Ca��OH��2��ϡ����������Һ | |
| B�� | ����BaCl2��Һ�����а취����NaOH��Na2CO3��Na2SO4 | |
| C�� | �з�̪��Һ�����ܼ������ᡢNa2CO3��KNO3������Һ | |
| D�� | ���������κ��Լ����ܽ�HCl��BaCl2��Na2CO3������Һ������� |
8�� ��ͬѧ��ΪCa��OH��2��CO2��Ӧ����NaOH��CO2���ܷ�Ӧ����Ϊʵ���������CO2��Ca��OH��2��Һ������NaOH��Һ����ͬѧ��Ϊ��ͬѧ��˵������ȫ��ȷ�����������ͬѧ�������ʵ����֤�����Ĺ۵㣮
��ͬѧ��ΪCa��OH��2��CO2��Ӧ����NaOH��CO2���ܷ�Ӧ����Ϊʵ���������CO2��Ca��OH��2��Һ������NaOH��Һ����ͬѧ��Ϊ��ͬѧ��˵������ȫ��ȷ�����������ͬѧ�������ʵ����֤�����Ĺ۵㣮
��1��[�������]��NaOH��CO2�ܷ�Ӧ
��2��[��Ʒ���]������ʯ��ʯ��ϡ������ȡCO2���壻
������ͼװ�ã�������ƿ�ǣ��뷢��װ����װ���ռ������CO2�����������������ƿƿ�����ϣ������������뵽����ƿ�ĵײ�
����֤����
���Լ��������
��4��[�ܽ��뷴˼]ʵ������NaOH��Һ�ױ��ʣ��仯ѧ����ʽΪ��2NaOH+CO2=Na2CO3+H2O������NaOH��ҺӦ�ܷⱣ�森
 ��ͬѧ��ΪCa��OH��2��CO2��Ӧ����NaOH��CO2���ܷ�Ӧ����Ϊʵ���������CO2��Ca��OH��2��Һ������NaOH��Һ����ͬѧ��Ϊ��ͬѧ��˵������ȫ��ȷ�����������ͬѧ�������ʵ����֤�����Ĺ۵㣮
��ͬѧ��ΪCa��OH��2��CO2��Ӧ����NaOH��CO2���ܷ�Ӧ����Ϊʵ���������CO2��Ca��OH��2��Һ������NaOH��Һ����ͬѧ��Ϊ��ͬѧ��˵������ȫ��ȷ�����������ͬѧ�������ʵ����֤�����Ĺ۵㣮��1��[�������]��NaOH��CO2�ܷ�Ӧ
��2��[��Ʒ���]������ʯ��ʯ��ϡ������ȡCO2���壻
������ͼװ�ã�������ƿ�ǣ��뷢��װ����װ���ռ������CO2�����������������ƿƿ�����ϣ������������뵽����ƿ�ĵײ�
����֤����
| ʵ�鲽�� | ʵ������ | ���� |
| ��һ��������CO2������ƿ��ע��������NaOH��Һ����ѡ�ø��ӣ��� | ƿ�ӱ���� | NaOH��Һ����������ƿ�е�CO2���壮 |
| �ڶ�����ȡ��һ����������Һ���������� | �д����������� | ��ѧ����ʽ��Na2CO3+2HCl�T2NaCl+H2O+CO2�� |
��4��[�ܽ��뷴˼]ʵ������NaOH��Һ�ױ��ʣ��仯ѧ����ʽΪ��2NaOH+CO2=Na2CO3+H2O������NaOH��ҺӦ�ܷⱣ�森
7�� ͭƬ�ڳ�ʪ�Ŀ����о��ã�����������ɫ��ͭ�⣮ijС��ͬѧ��Ʋ�����ʵ�飬̽��ͭ�����������
ͭƬ�ڳ�ʪ�Ŀ����о��ã�����������ɫ��ͭ�⣮ijС��ͬѧ��Ʋ�����ʵ�飬̽��ͭ�����������
����������衿�����£�ͭ���������O2��CO2��ˮ�����йأ�
������ʵ�顿ͨ��������ͭƬ�Ӵ������ʣ�������ͼװ�ã�ͭƬ��8cm����lcm���Թ��ݻ�Ϊ20mL�����ֱ��������7��ʵ�飬�������۲�30�죮
����������ۡ�
��1��ʵ��3�У�Ҫʹ�þ���в�Ѹ����ȴ������ˮ��ԭ���dz�ȥˮ�е�������
��2��ʵ��5��Ŀ����̽��ͭ�����Ƿ���ͭ��ˮ�Ͷ�����̼��ͬ��Ӧ�Ľ����
��3��ͨ������ʵ�飬�ó�ͭ�������������ˮ�������Ͷ�����̼��ͬ��Ӧ��
����˼�����ۡ�
��4����д��һ�ַ�ֹͭ��Ʒ��ʴ�ķ���Ϳ�ͣ�
��5���������Ͽ�֪��ͭ�����Ҫ�ɷ��Ǽ�ʽ̼��ͭ����ѧʽΪCu2��OH��2CO3���ɴˣ�����Ϊ����ʵ����ֻ�����ʵ��5��7����ʵ���ţ����Ϳ�̽����ͭ�������������i�Ǽ�ʽ̼��ͭ�Ļ�ѧʽ�к���̼����Ԫ�أ���Ԫ���غ����֪����ͭ����Ĺ�����һ���ж�����̼��ˮ�μӷ�Ӧ����ֻ��Ҫ����ʵ��5��7����֪��ͭ���������Ƿ���Ҫ�����IJμӣ�
��6�������Ͻ��е�ʵ��Աȣ�����ΪͭƬ��ͨ��״���Ŀ����У�����dz�������ԭ������ǿ�����������������̼��ˮ�����ĺ����ϵͣ�
 ͭƬ�ڳ�ʪ�Ŀ����о��ã�����������ɫ��ͭ�⣮ijС��ͬѧ��Ʋ�����ʵ�飬̽��ͭ�����������
ͭƬ�ڳ�ʪ�Ŀ����о��ã�����������ɫ��ͭ�⣮ijС��ͬѧ��Ʋ�����ʵ�飬̽��ͭ����������� ����������衿�����£�ͭ���������O2��CO2��ˮ�����йأ�
������ʵ�顿ͨ��������ͭƬ�Ӵ������ʣ�������ͼװ�ã�ͭƬ��8cm����lcm���Թ��ݻ�Ϊ20mL�����ֱ��������7��ʵ�飬�������۲�30�죮
| ��� | ��Ҫʵ����� | ʵ������ |
| 1 | ����������O2 | ͭƬ�������Ա仯 |
| 2 | ����������CO2 | |
| 3 | ��������в�Ѹ����ȴ������ˮ | |
| 4 | ��������ˮ5mL ��Һ��δ��ûͭƬ�����ٳ���O2 | |
| 5 | ���뾭��в�Ѹ����ȴ������ˮ5ml���ٳ���CO2 | |
| 6 | ����10mLO2���ٳ���10mLCO2 | |
| 7 | ��������ˮ5mL�������γ���l0mLCO2��10mLO2 | ͭƬ���⣬��ˮ�渽����ʴ������ |
��1��ʵ��3�У�Ҫʹ�þ���в�Ѹ����ȴ������ˮ��ԭ���dz�ȥˮ�е�������
��2��ʵ��5��Ŀ����̽��ͭ�����Ƿ���ͭ��ˮ�Ͷ�����̼��ͬ��Ӧ�Ľ����
��3��ͨ������ʵ�飬�ó�ͭ�������������ˮ�������Ͷ�����̼��ͬ��Ӧ��
����˼�����ۡ�
��4����д��һ�ַ�ֹͭ��Ʒ��ʴ�ķ���Ϳ�ͣ�
��5���������Ͽ�֪��ͭ�����Ҫ�ɷ��Ǽ�ʽ̼��ͭ����ѧʽΪCu2��OH��2CO3���ɴˣ�����Ϊ����ʵ����ֻ�����ʵ��5��7����ʵ���ţ����Ϳ�̽����ͭ�������������i�Ǽ�ʽ̼��ͭ�Ļ�ѧʽ�к���̼����Ԫ�أ���Ԫ���غ����֪����ͭ����Ĺ�����һ���ж�����̼��ˮ�μӷ�Ӧ����ֻ��Ҫ����ʵ��5��7����֪��ͭ���������Ƿ���Ҫ�����IJμӣ�
��6�������Ͻ��е�ʵ��Աȣ�����ΪͭƬ��ͨ��״���Ŀ����У�����dz�������ԭ������ǿ�����������������̼��ˮ�����ĺ����ϵͣ�
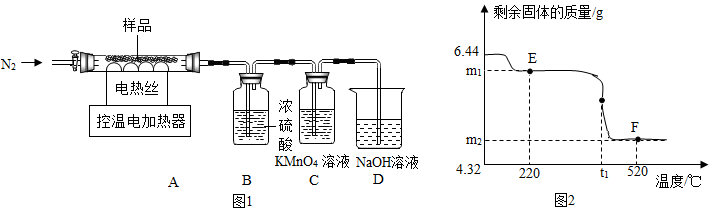
6�����㸡�顱��Ҫ�ɷ��ǹ�̼���ƣ�xNa2CO3•yH2O2�����׳ƹ���˫��ˮ����ȤС������������̽����
������̽����
��1��ȡ�������㸡�顱���Թ��м�ˮ���г���ϸС���ݻ����ų������Թ��м�������MnO2��ĩ�������������ݣ���������ľ�������Թܣ�ľ����ȼ��˵����O2���ɣ�
��2��ȡʵ�飨1�����ϲ���Һ�������ҺPH��7������Һ�еμ�����ϡ���ᣬ�����������ݣ�������������ͨ�����ʯ��ˮ�У����ֻ�������˵����CO2���������̼�����ɣ�
���ۣ���̼���ƾ���Na2CO3��H2O2��˫�ػ�ѧ���ʣ�
����ҵ�Ʊ���
��3������������ݣ�����Ϊ�����Ʊ���Ӧ������¶ȷ�Χ��15��20�森
ע��������������ָ��Ʒ����ת��ΪO2����Ԫ�ص�����������
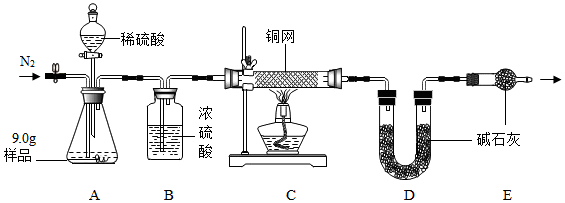
����ɲⶨ��������ͼװ�ý��в�Ʒ�л����������ⶨ��̼���ƣ�xNa2CO3•yH2O2����ɵIJⶨ�����ʶԲⶨ��Ӱ�죩
�������ϣ��١��㸡�顱�л�����������13.0%��һ��Ʒ����10.5%�Ǻϸ�Ʒ���ڹ�̼���������ᷴӦ�ų�CO2��O2��
��4��ʵ��ǰ�Ȼ���ͨN2һ��ʱ�䣬����ͭ�������Ⱥ��ٻ����������ϡ���ᣬֱ��A����Ʒ��ȫ��Ӧ����������ͨN2����Ŀ���ǽ����ɵ�O2��CO2����װ��C��D��ʹ�䱻��ȫʹ������װ���е�����ȫ�������գ�
��5�����ȵ���ϡ���ᣬ�����ͭ�����ᵼ��x��y��ֵƫ���ƫ��ƫС������
��6��ʵ����Cװ����ͭ������1.2g��Dװ������2.2g���ò�Ʒ�л���������Ϊ12%�����ںϸ�Ʒ���һ��Ʒ�����ϸ�Ʒ�����ϸ�Ʒ������
������̽����
��1��ȡ�������㸡�顱���Թ��м�ˮ���г���ϸС���ݻ����ų������Թ��м�������MnO2��ĩ�������������ݣ���������ľ�������Թܣ�ľ����ȼ��˵����O2���ɣ�
��2��ȡʵ�飨1�����ϲ���Һ�������ҺPH��7������Һ�еμ�����ϡ���ᣬ�����������ݣ�������������ͨ�����ʯ��ˮ�У����ֻ�������˵����CO2���������̼�����ɣ�
���ۣ���̼���ƾ���Na2CO3��H2O2��˫�ػ�ѧ���ʣ�
����ҵ�Ʊ���
��3������������ݣ�����Ϊ�����Ʊ���Ӧ������¶ȷ�Χ��15��20�森
| �¶ȷ�Χ/�� | 5��10 | 10��15 | 15��20 | 20��25 |
| ����������/% | 13.94 | 14.02 | 15.05 | 14.46 |
| ���㸡�顱�IJ���/% | 85.49 | 85.78 | 88.38 | 83.01 |
����ɲⶨ��������ͼװ�ý��в�Ʒ�л����������ⶨ��̼���ƣ�xNa2CO3•yH2O2����ɵIJⶨ�����ʶԲⶨ��Ӱ�죩
�������ϣ��١��㸡�顱�л�����������13.0%��һ��Ʒ����10.5%�Ǻϸ�Ʒ���ڹ�̼���������ᷴӦ�ų�CO2��O2��
��4��ʵ��ǰ�Ȼ���ͨN2һ��ʱ�䣬����ͭ�������Ⱥ��ٻ����������ϡ���ᣬֱ��A����Ʒ��ȫ��Ӧ����������ͨN2����Ŀ���ǽ����ɵ�O2��CO2����װ��C��D��ʹ�䱻��ȫʹ������װ���е�����ȫ�������գ�
��5�����ȵ���ϡ���ᣬ�����ͭ�����ᵼ��x��y��ֵƫ���ƫ��ƫС������
��6��ʵ����Cװ����ͭ������1.2g��Dװ������2.2g���ò�Ʒ�л���������Ϊ12%�����ںϸ�Ʒ���һ��Ʒ�����ϸ�Ʒ�����ϸ�Ʒ������

5��ijͬѧ���ʵ��̽������ͭ�������ֽ����Ļ��˳����������ĸ�ʵ�鷽�����ֱ�ѡ����Լ��ǣ���ͭ����������������Һ����������������ͭ��Һ������������������Һ������ͭ��Һ����ͭ������������Һ����������Һ�������ĸ�������ѡ�Լ���ȷ��2���Ǣڢܣ�������������1���Լ����ʵ��������
0 154700 154708 154714 154718 154724 154726 154730 154736 154738 154744 154750 154754 154756 154760 154766 154768 154774 154778 154780 154784 154786 154790 154792 154794 154795 154796 154798 154799 154800 154802 154804 154808 154810 154814 154816 154820 154826 154828 154834 154838 154840 154844 154850 154856 154858 154864 154868 154870 154876 154880 154886 154894 211419
| ʵ�鲽�� | ���� | ���ۼ���ѧ����ʽ |
| �� �� | ������ߵĻ�ԣ�����ͭ���� |
 ��ѧ��ȤС���Ա��һ����̼��ԭ������ʵ��������ɫ���Ľ�����ȡ��������ͼ
��ѧ��ȤС���Ա��һ����̼��ԭ������ʵ��������ɫ���Ľ�����ȡ��������ͼ ��ѧ��ȤС�������������������̽����
��ѧ��ȤС�������������������̽����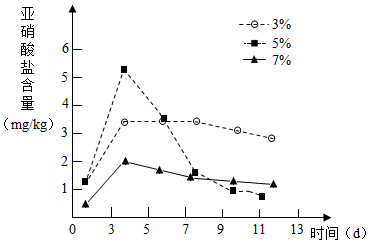 ����ݲ��ڷ������л�����������Σ��°����ʣ�����ʵ��ij�С�����ʵ�飬̽����ͬʳ��Ũ�Ⱥͷ���ʱ����������κ����仯��Ӱ�죬��ش�
����ݲ��ڷ������л�����������Σ��°����ʣ�����ʵ��ij�С�����ʵ�飬̽����ͬʳ��Ũ�Ⱥͷ���ʱ����������κ����仯��Ӱ�죬��ش�