��Ŀ����
4�������������仯�����ʵ��̽������ش�������⣺�������
��1���Գ�����Ϊԭ��ұ�����Ļ�ѧ��Ӧ����ʽΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��2����Fe������ϡH2SO4�Ļ�ѧ����ʽ��Fe+H2SO4�TFeSO4+H2�����˷�Ӧ�����û���Ӧ���������Ӧ���ͣ����õ�ȼ���������ɵ�H2ǰ�����鴿����������Ӧ�����Һ�еμ�NaOH��Һ�����ɰ�ɫFe��OH��2��������������Ϊ����ɫ����ɫ������Ϊ����ɫ��ԭ��֮һ�Dz���Fe��OH��2��ʪ��Ŀ���������Fe��OH��3���䷴Ӧ�Ļ�ѧ����ʽ4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���������ɫ������ȷֽ�ʵ��
���ˡ�ϴ�ӡ����¸���õ�����ɫ���壬�����Ϊ2FeSO4•2Fe��OH ��2•Fe2O3[��Է�������Ϊ644]����ȤС���ȡ�˻���ɫ����6.44g���ڿ�����Ա��ָ������ͼ1װ�ý����ȷֽ�ʵ�飮
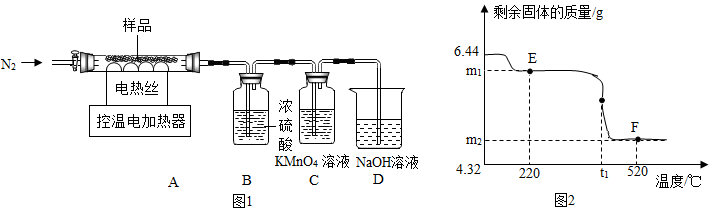
���������ϡ���Fe��OH��2��150�桫200��ʱ��ȫ�ֽ�ΪFeO��
��FeSO4��450�桫500��ʱ��ȫ�ֽ�ΪFe2O3��
��2FeSO4$\frac{\underline{\;450��-500��\;}}{\;}$Fe2O3+SO2��+SO3��
��Ũ����ֻ������SO3��H2O��
��SO2��ʹKMnO4��Һ��ɫ
��1������ǰ�����о�ͨ��N2������ǰͨN2��Ŀ���ǽ�װ���ڵĿ����ϳ���
��2�������¶��ڲ�ͬ�ķ�Χ��A����Ʒ���ȣ����ʣ������������¶ȵı仯��ͼ2��ʾ��
�ٵ����ȵ�t1��ʱ��װ��C�е���Һ��ɫ����ͨ�뵽װ��C�е�����ΪSO2�������ѧʽ����
��ͼ��E���Ӧ��ml=6.08��
��ͼ��F���Ӧ������Fe2O3������Ϊ3.2g��
�ܿ�����Ա��F������ʣ�����������������ܱ������м��ȵ�1400�棬�õ������Ĵ���Fe3O4����֪���ȹ����з���������Ӧ���ҷ�Ӧǰ��������������䣮��д������һ����Ӧ�Ļ�ѧ����ʽFe2O3+FeO$\frac{\underline{\;����\;}}{\;}$Fe3O4��
���� �������1�����ݻ�ѧ����ʽ����д���������裨д���䡢ע���ȣ�������д���ɣ���2������������Ϣ�����ѧ��ѧ֪ʶ���з�����
��������ݼ���ǰװ�����п��������������ݸ�����ؾ���������������������2FeSO4•2Fe��OH��2•Fe2O3�е������������ֽ�ΪFeO������������FeSO4������������Fe2O3�����������������Ϣ���������
��� �⣺�������
��1����һ����̼��ԭ��������������Ҫ������CO�Ļ�ԭ�ԣ��ڸ����º���������Ӧ�������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2�����Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��2����Fe������ϡH2SO4�Ļ�ѧ����ʽ��Fe+H2SO4�TFeSO4+H2�����˷�Ӧ�ķ�Ӧ����һ�ֵ��ʺ�һ�ֻ������������һ�ֵ��ʺ�һ�ֻ���������û���Ӧ���õ�ȼ���������ɵ�H2ǰ�����鴿��Fe��OH��2��ʪ��Ŀ���������Fe��OH��3���䷴Ӧ�Ļ�ѧ����ʽ��4Fe��OH��2+O2+2H2O�T4Fe��OH��3�����Fe+H2SO4�TFeSO4+H2�����û���Ӧ���鴿��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�������1������ǰ��ͨ��һ��ʱ��N2��Ŀ���ǽ�װ���ڵĿ����ϳ�����ֹ��������������Ϊ���������������װ���ڵĿ����ϳ���
��2���ٵ����ȵ�t1��ʱ��������ؾ��������ԣ������ն���������Һ���Ϻ�ɫ��dz����ͨ�뵽װ��C�е�����ΪSO2�����SO2��
��ͼ2��E���Ӧ��m1Ϊ2FeSO4•2Fe��OH��2•Fe2O3�е������������ֽ�ΪFeO��ʣ������������������ˮ������Ϊx
2FeSO4•2Fe��OH��2•Fe2O3--2H2O
644 36
6.44g x
$\frac{644}{36}$=$\frac{6.44g}{x}$��x=0.36g
��m1=6.44g-0.36g=6.08g�����6.08��
��������Fe2O3������Ϊy��
6.44g2FeSO4•2Fe��OH��2•Fe2O3�к���FeSO4������Ϊ��6.44g��$\frac{152��2}{644}$=3.04g
6.44g2FeSO4•2Fe��OH��2•Fe2O3�к���Fe2O3������Ϊ��6.44g��$\frac{160}{644}$=1.6g
2FeSO4$\frac{\underline{\;450�桫500��\;}}{\;}$Fe2O3+SO2��+SO3��
304 160
3.04g y
$\frac{304}{160}$=$\frac{3.04g}{y}$
ͼ2��F���Ӧ������Fe2O3������Ϊ1.6g+1.6g=3.2g�����3.2��
�������������������ڸ��µ������·�Ӧ���������������������Fe2O3+FeO$\frac{\underline{\;����\;}}{\;}$Fe3O4��
���� �����ۺϿ����˽����Ļ�ԡ����ϵķ��ࡢ������ұ���������ķ��⡢���ʵ��Ʊ�������һ�����Ѷȣ����ʱҪ������ѧ֪ʶ����������Ϣ����������

| A�� | ������������ѹ���ں�С����ɫ��ƿ��-------���Ӽ��м�� | |
| B�� | �����б�������ú��й©-------�����ڲ����˶� | |
| C�� | ���ȱ��ƹ�������ˮ�лָ�ԭ״-------���ӵ������� | |
| D�� | ˮ��ͨ����������������������-------�⡢��ԭ��������� |
| A�� | Ũ���������ˮ�ԣ�����Ũ����Ҳ������ˮ�� | |
| B�� | �����pHС��7������pHС��7����ˮһ�������� | |
| C�� | �����Ǵ���ɵ��������Դ���ɵ���һ�������� | |
| D�� | ���CO��CO2��Ԫ����ͬ�������ǵķ��ӹ��ɲ�ͬ���������ǵĻ�ѧ���ʲ�ͬ |
| A�� | Al3+-��Ԫ�صĻ��ϼ�Ϊ+3 | |
| B�� | 3H2O-3��ˮ���� | |
| C�� | 3H-3����ԭ�� | |
| D�� | SO3-1��������������к���3����ԭ�� |
| A�� |  | B�� |  | C�� |  | D�� |  |
 ��ͼ�г������ϵ�Ӫ���ɷ֣�
��ͼ�г������ϵ�Ӫ���ɷ֣�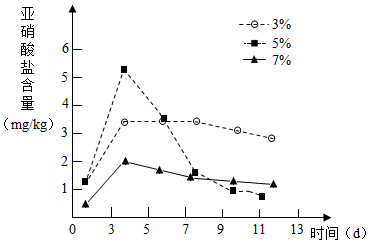 ����ݲ��ڷ������л�����������Σ��°����ʣ�����ʵ��ij�С�����ʵ�飬̽����ͬʳ��Ũ�Ⱥͷ���ʱ����������κ����仯��Ӱ�죬��ش�
����ݲ��ڷ������л�����������Σ��°����ʣ�����ʵ��ij�С�����ʵ�飬̽����ͬʳ��Ũ�Ⱥͷ���ʱ����������κ����仯��Ӱ�죬��ش�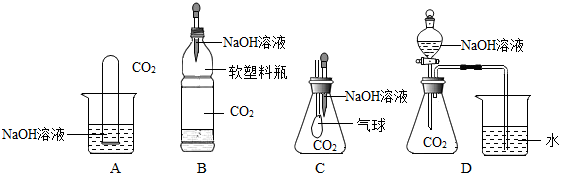
 ͨ�����ˮʵ������о�ˮ����ɣ����ˮ��װ������ͼ3��ʾ���÷�Ӧ�Ļ�ѧ����ʽ��2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
ͨ�����ˮʵ������о�ˮ����ɣ����ˮ��װ������ͼ3��ʾ���÷�Ӧ�Ļ�ѧ����ʽ��2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����