题目内容
2. 双福育才中学农场的工作人员会在长途运输鱼苗时,向水中加入少量过氧化钙(CaO2)固体.小明、小红两位同学发现往水中投入过氧化钙时产生气泡.
双福育才中学农场的工作人员会在长途运输鱼苗时,向水中加入少量过氧化钙(CaO2)固体.小明、小红两位同学发现往水中投入过氧化钙时产生气泡.【提出问题】当把过氧化钙投入足量水中时,最终生成什么物质?
【进行猜想】小明:生成氧化钙和氧气; 小红:生成氢氧化钙和氧气.
你赞同的猜想是小红(填“小明”或“小红”),其理由是质量守恒定律或化学反应前后元素的种类不变;
【查阅资料】氢氧化钙溶解在水中可以形成澄清石灰水.
【实验探究】
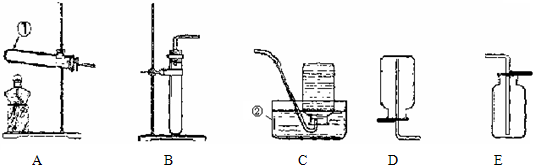
(1)打开如图装置中分液漏斗的活塞,控制滴加水速度,观察到试管内有气泡产生.
①将一根带火星的小木条放在导气管口P处,若复燃(填实验操作和实验现象),说明生成的气体是氧气.
②实验过程中,发现烧杯中有气泡出现,该现象说明该反应会放热.
(2)请设计一个实验方案来验证小红同学猜想的生成物中有“氢氧化钙”:
| 实验步骤及操作方法 | 预期的实验现象 | 结论 |
| ①取少量过氧化钙放入试管中,加足量水,振荡, ②取上层清液通入二氧化碳 | ①产生气泡, ②液体变浑浊或产生白色沉淀. | 过氧化钙和水反应产生的另一种物质是氢氧化钙 |
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是增加水中含氧量;
(2)过氧化钙和水反应的化学方程式为2CaO2+2H2O═2Ca(OH)2+O2↑.
分析 【进行猜想】对反应生成物进行猜测时,应考虑到当前条件下,所猜测的物质能否稳定存在.换句话说,在当前条件下是否有物质还可以与所猜测物质继续反应.判断两位同学猜想孰对孰错,将两位同学的猜想进行对比,发现二人的猜想差异:生成物中是否含氢元素?确定了氢元素也就有是对错的结果.
【实验探究】根据氧气的检验方法以及反应过程中放出热量来分析;
向反应后的溶液中通入二氧化碳气体,溶液变浑浊,有氢氧化钙生成;
【问题讨论】过氧化钙遇水放出氧气,巧妙地解决了运输鱼苗过程水中氧气不足的问题;
经过以上探究可知,过氧化钙与水反应生成氢氧化钙和氧气.
解答 解:【进行猜想】小明同学猜想中的氧化钙不可能在水中存在,因为氧化钙能与水反应生成氢氧化钙.所以小明的猜想错误.也可根据质量守恒定律,变化前后元素种类不变,而小明同学的猜想中少了氢元素,不符合质量守恒定律,所以小明的猜想错误.
故答答案为:小红;质量守恒定律或化学反应前后元素的种类不变;
【实验探究】(1)①氧气具有助燃性,能使带火星的木条复燃,所以可将一根带火星的小木条放在导气管口P处,若复燃证明是氧气;故填:将一根带火星的小木条放在导气管口P处,若复燃;
②反应放热,造成装置内气体体积膨胀,导管冒出气泡;故填:该反应会放热;
(2)向反应后的溶液中通入二氧化碳气体,溶液变浑浊,说明有氢氧化钙生成,故答案为:液体变浑浊或产生白色沉淀;
【问题讨论】(1)过氧化钙与水反应放出氧气,恰好补充了鱼苗运动过程中水中氧气的消耗.故答案为:增加水中含氧量;
(2)过氧化钙与水反应后生成了氢氧化钙,同时放出氧气.故填:2CaO2+2H2O═2Ca(OH)2+O2↑.
点评 实验探究题是近几年中考的重点内容之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等,还考查了化学方程式的书写等.本题通过查阅资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握,本考点主要出现在实验题中.

| A. | Na2CO3、HCl、CaCl2、HNO3 | B. | FeCl3、NaOH、Na2SO4、KCl | ||
| C. | KNO3、HCl、NaOH、FeCl3 | D. | NH4Cl、KOH、Na2SO4、BaCl2 |
| A. | 氧气与臭氧(O3)的化学性质不同,是因为它们是由不同的分子构成 | |
| B. | 用明火检验燃气是否泄漏 | |
| C. | 过滤或加热均能使硬水转化为软水 | |
| D. | 可燃冰就是干冰,主要成分是CO2 |

| A. | 参加反应的A和B的分子个数比是1:2 | |
| B. | A分子聚集成的物质的化学性质由A分子保持 | |
| C. | D分子一定改变了该反应的反应速率 | |
| D. | C分子聚集成的物质可能是氧化物 |
| A. | 中子数 | B. | 质子数 | C. | 核外电子数 | D. | 相对原子质量 |
| A. |  | B. |  | ||
| C. |  | D. |  |
| A. | H2 | B. | CH4 | C. | CO2 | D. | CO |