题目内容
8.在一次用餐中,同学们对燃料“固体酒精”产生了好奇.于是对其成分进行探究.【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
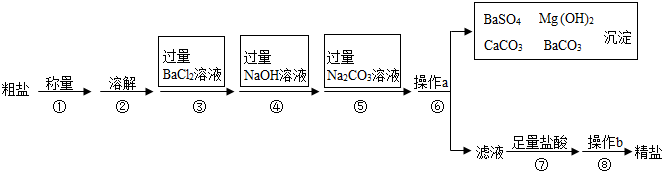
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
| 方案 | 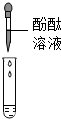 | 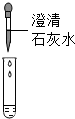 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
分析 【实验探究】(1)根据氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳分析;
(2)根据碳酸钠能和氢氧化钙反应产生碳酸钙沉淀分析现象;
(3)根据氢氧化钠溶液和碳酸钠溶液都显碱性,都能够使酚酞试液变红色分析;
【反思交流】(4)为了使碳酸钠完全反应,应该加入过量的氯化钡溶液;
【拓展应用】(5)碳酸钠能和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠分析;
解答 解:【实验探究】(1)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,因此白色沉淀是碳酸钠和氯化钙反应生成的碳酸钙,碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)碳酸钠能和氢氧化钙反应产生碳酸钙沉淀,故填:白色沉淀;
(3)乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是:碳酸钠溶液显碱性,也能使酚酞试液变红色.
(4)乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
(5)要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的氢氧化钡溶液、氢氧化钙溶液,不能选择氯化钙溶液,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此使用氯化钙时能够带入新杂质--氯化钠.故填:AC;
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)①白色沉淀;②Na2CO3溶液呈碱性,也能使酚酞变红;
[反思交流]除去溶液中的Na2CO3,排除其对NaOH检验的干扰;
[拓展应用]AC
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

| A. | 芝麻油可溶于水形成溶液 | |
| B. | 析出晶体后的溶液可能是不饱和溶液 | |
| C. | 20℃时,硝酸钾的饱和溶液不能再溶解其他物质 | |
| D. | 20℃时,氢氧化钙的饱和溶液一定比其不饱和溶液浓度大 |
| A. | 配制时,用50mL量筒分两次共量取95.0mL水 | |
| B. | 配制时,将NaOH固体放入小烧杯,用托盘天平称取5.0g NaOH固体 | |
| C. | 用pH试纸可以测得溶液的pH=13.7 | |
| D. | 100mL 5% NaOH溶液中加入100mL水得到2.5% NaOH溶液 |
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 硫在氧气中燃烧产生苍白色火焰 | |
| C. | 木炭在氧气中燃烧发出白光,生成的无色气体能使澄清的石灰水变浑浊 | |
| D. | 镁在空气中燃烧,发出耀眼的白光,生成白色固体 |
| A. | 可燃性 | B. | 在常温下,化学性质不活泼 | ||
| C. | 还原性 | D. | 吸附性 |
 甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t2℃时甲的溶解度大于乙 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 | |
| C. | t2℃时,将等质量的甲、乙两物质加水溶解配成饱和溶液,所得溶液的质量甲<乙 | |
| D. | t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 |