题目内容
17. 甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t2℃时甲的溶解度大于乙 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 | |
| C. | t2℃时,将等质量的甲、乙两物质加水溶解配成饱和溶液,所得溶液的质量甲<乙 | |
| D. | t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 |
分析 A、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
B、等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多;
C、据该温度下两物质的溶解度大小分析解答;
D、该温度下二者的溶解度相等,则等质量的饱和溶液中含有溶质的质量相等.
解答 解:A、由图可知:t2℃时甲的溶解度大于乙,正确;
B、等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多,现在不知两溶液的质量,故无法比较降温析出晶体的质量多少,故错误;
C、t2℃时甲的溶解度大于乙,则将等质量的甲、乙两物质加水溶解配成饱和溶液,乙需要水的质量多,故所得溶液的质量甲<乙,正确;
D、该温度下二者的溶解度相等,则t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等,正确;
故选:B.
点评 了解溶解度概念的含义、溶解度曲线的相关知识,才能结合题意灵活分析解答.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
7.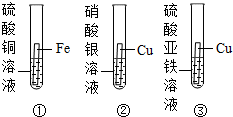 如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
 如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )| A. | ①铁片表面无明显变化 | |
| B. | ③溶液逐渐变蓝色 | |
| C. | 通过该实验能得出:金属活动性顺序为:Fe>H>Cu>Ag | |
| D. | ①②或②③都能得出金属活动性顺序为:Fe>Cu>Ag |
8.在一次用餐中,同学们对燃料“固体酒精”产生了好奇.于是对其成分进行探究.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠.理由是Na2CO3溶液呈碱性,也能使酚酞变红.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后过滤,向滤液中滴加酚酞溶液,酚酞溶液变红.
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
| 方案 | 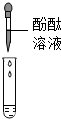 | 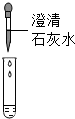 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
12. 在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
 在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )| A. | 铈属于非金属元素 | B. | 铈的原子序数是58 | ||
| C. | 铈原子中的质子数是50 | D. | 铈的相对原子质量是140.1g |
2.某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥,过程如图所示,其中试剂甲和乙可能是( )


| A. | 甲:水,乙:氢氧化钠 | B. | 甲:氯化钠,乙:稀硫酸 | ||
| C. | 甲:稀盐酸,乙:氯化钠溶液 | D. | 甲:熟石灰,乙:稀盐酸 |
19.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
| A. | 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | |
| B. | 水和过氧化氢的组成元素相同,则两者的化学性质相同 | |
| C. | 碱在组成上都含有氢氧根,则Cu2(OH)2CO3有氢氧根也是碱 | |
| D. | 单质由同种元素组成,所以由同种元素组成的纯净物一定是单质 |

 人体缺少钙元素会影响健康,因此每日需摄人足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算.
人体缺少钙元素会影响健康,因此每日需摄人足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算.