题目内容
19.溶液与我们的生活息息相关,下面有关溶液的说法正确的是( )| A. | 芝麻油可溶于水形成溶液 | |
| B. | 析出晶体后的溶液可能是不饱和溶液 | |
| C. | 20℃时,硝酸钾的饱和溶液不能再溶解其他物质 | |
| D. | 20℃时,氢氧化钙的饱和溶液一定比其不饱和溶液浓度大 |
分析 A、根据芝麻油不溶于水考虑;B、析出晶体后的溶液一定是该种溶质的饱和溶液;C、某种溶质的饱和溶液可以溶解其他物质;D、同一温度、同一溶质饱和溶液比不饱和溶液浓度大.
解答 解:
A、芝麻油不溶于水,与水混合形成的是乳浊液,故A错;
B、析出晶体后的溶液一定是该种溶质的饱和溶液,故B错;
C、某种溶质的饱和溶液可以溶解其他物质,故C错;
D、同一温度、同一溶质饱和溶液比不饱和溶液浓度大,故D正确.
故选D.
点评 溶液是均一、稳定的混合物,要知道同一温度、同一溶质饱和溶液比不饱和溶液浓度大.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 固体物质在100g水中最多能溶解多少克,它的溶解度就是多少克 | |
| B. | 搅拌、振荡可以加快物质溶解的速率,但不能使它的溶解度增大 | |
| C. | 大部分固体的溶解度与温度成正比 | |
| D. | 固体、气体的溶解度一般都随温度的升高而增大 |
7.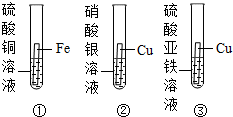 如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
 如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )
如图是金属活动性探究实验的一部分,有关该实验的说法中正确的是( )| A. | ①铁片表面无明显变化 | |
| B. | ③溶液逐渐变蓝色 | |
| C. | 通过该实验能得出:金属活动性顺序为:Fe>H>Cu>Ag | |
| D. | ①②或②③都能得出金属活动性顺序为:Fe>Cu>Ag |
4.中国载人航天工程总设计师周建平表示,我国天宫二号空间实验室将于2016年发射.天宫二号是在天宫一号目标飞行器备份的基础上,根据天宫二号任务的需要改装研制而成的.某校化学兴趣小组同学查阅资料得知“天宫一号”目标飞行器制作材料有铝、耐高温的石墨瓦、不锈钢、钛和铜等.
(1)将铁制成不锈钢可以提高铁的抗腐蚀能力,生活中还常使用在铁制品表面刷漆防止铁生锈.
(2)同学们设计了如下实验探究了Fe、Al、Cu三种金属的活动性顺序:
【反思交流】
方案二中发生的反应用化学方程式表示为Fe+CuSO4=Cu+FeSO4;Al比Fe活泼,但Al不易生锈,其原因是Al在空气中表面形成了一层致密的氧化膜,阻止了Al和氧气持续反应.
(1)将铁制成不锈钢可以提高铁的抗腐蚀能力,生活中还常使用在铁制品表面刷漆防止铁生锈.
(2)同学们设计了如下实验探究了Fe、Al、Cu三种金属的活动性顺序:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取用砂纸打磨光亮且大小形状相同的三种种金属片于3支试管中,分别加入等质量、同浓度的稀盐酸(稀硫酸)溶液 | Fe与Al表面均产生气体,Al产生氢气的速率大于Fe铜表面无气泡产生. | 活动性顺序:Al>Fe>Cu |
| 方案二 | 取用砂纸打磨光亮且大小相等的Fe片于2去试管中,分别加入适量Al2(SO4)3、CuSO4溶液 | Al2(SO4)3溶液中Fe片及溶液均无明显变化:CuSO4溶液中Fe片表面析出红色物质,溶液变为浅绿色 |
方案二中发生的反应用化学方程式表示为Fe+CuSO4=Cu+FeSO4;Al比Fe活泼,但Al不易生锈,其原因是Al在空气中表面形成了一层致密的氧化膜,阻止了Al和氧气持续反应.
11.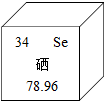 西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
 西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )| A. | 硒元素属于金属元素 | B. | 硒元素的相对原子质量为78.96g | ||
| C. | 硒元素的原子序数为34 | D. | 硒原子核内有78个质子 |
8.在一次用餐中,同学们对燃料“固体酒精”产生了好奇.于是对其成分进行探究.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠.理由是Na2CO3溶液呈碱性,也能使酚酞变红.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后过滤,向滤液中滴加酚酞溶液,酚酞溶液变红.
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
| 方案 | 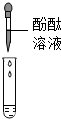 | 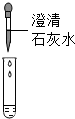 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
 人体缺少钙元素会影响健康,因此每日需摄人足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算.
人体缺少钙元素会影响健康,因此每日需摄人足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算.