题目内容
3.据报道,“染色”馒头中添加柠檬黄铬酸铅(PbCrO4)会使人致癌,已被文明禁用.已知该物质中铅元素(Pb)的化合价为+2,则铬元素的化合价为( )| A. | +4 | B. | +5 | C. | +6 | D. | +7 |
分析 根据在化合物中正负化合价代数和为零,结合柠檬黄铬酸铅(PbCrO4)的化学式进行解答本题.
解答 解:铅元素的化合价为+2价,氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×4=0,则x=+6价.
故选C.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
11.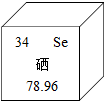 西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
 西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )
西瓜里富含硒元素,硒被誉为“抗癌大王”,如图是硒元素在元素周期表中的部分信息.下列说法正确的是( )| A. | 硒元素属于金属元素 | B. | 硒元素的相对原子质量为78.96g | ||
| C. | 硒元素的原子序数为34 | D. | 硒原子核内有78个质子 |
18.下列变化中,属于化学变化的是( )
| A. | 铁生锈 | B. | 冰雪融化 | ||
| C. | 因电压过高,灯泡烧坏 | D. | 分离液态空气 |
8.在一次用餐中,同学们对燃料“固体酒精”产生了好奇.于是对其成分进行探究.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠.理由是Na2CO3溶液呈碱性,也能使酚酞变红.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后过滤,向滤液中滴加酚酞溶液,酚酞溶液变红.
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
【查阅资料】:(1)该固体酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液呈中性.
【提出问题】:固体酒精中的氢氧化钠是否变质?
【实验探究】:(1)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
分析实验并结合资料得出氢氧化钠已变质.
(2)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
| 方案 | 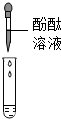 | 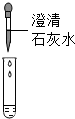 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】:经过讨论一致认为固体酒精中氢氧化钠部分变质.
【反思交流】:乙组实验中加足量氯化钡溶液的目的是除去溶液中的Na2CO3,排除其对NaOH检验的干扰.
【拓展应有】:要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
15.为了验证铁、锌、铜三种金属的活动性顺序,某同学设计了下列四种方案,其中一定能达到实验目的是( )
| A. | 将Zn、Cu分别加入到FeSO4溶液中 | |
| B. | 把Zn分别加入到CuSO4溶液、FeSO4溶液中 | |
| C. | 把Zn、Cu分别加入到ZnSO4溶液中 | |
| D. | 把Cu分别加入到FeSO4溶液、ZnSO4溶液中 |
12. 在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
 在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )
在元素周期表中铈(Ce)元素的某些信息如图所示,下列有关铈的说法正确的是( )| A. | 铈属于非金属元素 | B. | 铈的原子序数是58 | ||
| C. | 铈原子中的质子数是50 | D. | 铈的相对原子质量是140.1g |
13.日本福岛发生核泄漏事故,核电站泄漏出来的放射性物质中含有铯-137.已知铯-137的质子数为55,中子数为82,下列有关铯-137的说法正确的是( )
| A. | 原子的核外电子数为82 | B. | 相对原子质量为137g | ||
| C. | 核电荷数为55 | D. | 属于非金属元素 |
 下列概念符合图关系的是( )
下列概念符合图关系的是( )