题目内容
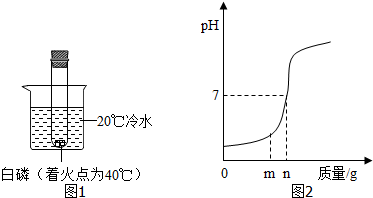
10. (1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)
(1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)(2)该反应发生变化的微粒是氢离子和氢氧根离子
(3)任写出一个酸和碱有明显现象的反应化学方程式H2SO4+Ba(OH)2═BaSO4↓+2H2O.
分析 (1)根据碱能使无色酚酞变红,酸碱能发生中和反应,观察图示情况解答即可;
(2)根据氢氧化钠与盐酸恰好完全反应,溶液呈中性解答;
(3)根据氢氧化钡和硫酸反应生成硫酸钡白色沉淀解答.
解答 解:
(1)由第二步烧杯中液体变为红色可知,①中试剂为碱NaOH溶液,②中为酚酞;
(2)氢氧化钠与盐酸恰好完全反应,溶液呈中性,该反应发生变化的微粒是氢离子和氢氧根离子;
(3)硫酸是强酸,氢氧化钡是强碱,二者之间发生中和反应生成硫酸钡和水,方程式为:H2SO4+Ba(OH)2═BaSO4↓+2H2O,
答案:
(1)氢氧化钠溶液、酚酞;
(2)氢离子和氢氧根离子;
(3)H2SO4+Ba(OH)2═BaSO4↓+2H2O.
点评 要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,综合分析并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
1.现有①铁锈;②铁水;③锰钢;④纯碱;⑤烧碱;⑥小苏打;⑦干冰;⑧石灰水;⑨生石灰等物质.
下列有关物质的分类中正确的是( )
下列有关物质的分类中正确的是( )
| A. | 盐--④⑤⑥ | B. | 氧化物--①⑦⑨ | C. | 碱--④⑤⑧ | D. | 混合物--①③⑧ |
18.一同学用某种粗盐进行提纯实验,步骤见图.

请回答:
(1)步骤①和②的操作名称是过滤.
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡放出为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成固体(或溶液)飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:

请回答:
(1)步骤①和②的操作名称是过滤.
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡放出为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成固体(或溶液)飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 有气泡放出,石灰水变浑浊 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想II不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量制得的NaCl晶体溶于试管中的蒸馏水,滴入BaCl2 | 有白色沉淀 | 猜想Ⅲ成立 |
2.2016唐山世界园艺博览会的主题为“都市与自然•凤凰涅槃”,作为唐山市民应践行绿色生活,你认为下列做法错误的是( )
| A. | 尽量少开私家车 | B. | 用布袋代替塑料袋购物 | ||
| C. | 夏季空调温度尽量低些 | D. | 垃圾分类回收 |

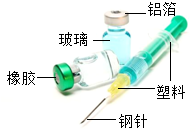 如图所示是医院常用的药瓶和注射器,请你据图回答:
如图所示是医院常用的药瓶和注射器,请你据图回答: