题目内容
20.请回答如图所示两个实验中的相关问题.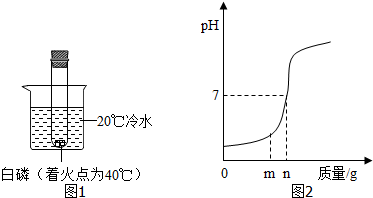
(1)实验装置如图1所示,往烧杯中加入一定量生石灰会引起白磷燃烧.
①此时生石灰的作用是生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.
②若将一定量的浓硫酸、氢氧化钠(填两种物质)加入烧杯中的冷水,也能引起白磷燃烧.
(2)用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图2所示.当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用ng氢氧化钠与相同量盐酸反应,所得溶液的pH<7(填“>“、“<“或“=”).
分析 (1)根据生石灰与水的反应分析回答;物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,据此分析.
(2)根据质量守恒定律可以书写化学方程式,根据化学方程式和图中情况可以进行相关方面的计算.
解答 解:(1)往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是:生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.将一定量的下列某物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,浓硫酸、氢氧化钠在溶于水时能放出热量,能使溶液的温度升高.
(2)氢氧化钙和盐酸反应能生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H20,
当加入熟石灰mg时,盐酸有剩余,溶液中的溶质是盐酸中的氯化氢和反应生成的氯化钙.故填:CaCl2和HCl.
由Ca(OH)2+2HCl=CaCl2+2H20; NaOH+HCl═NaCl+H2O 可知,氢氧化钙和盐酸反应的质量比是74:73.氢氧化钠和盐酸反应的质量比是80:73.加入ng氢氧化钙恰好完全反应,溶液显中性.加入ng氢氧化钠不能把盐酸反应完,即盐酸过量,溶液显酸性,PH<7.故填:<
故答案为:
(1)生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点,浓硫酸、氢氧化钠;
(2)CaCl2和HCl;<.
点评 本题考查了燃烧的条件,明确物质溶于水或与水反应是否放热来分析.主要考查了化学方程式的书写及其根据图中信息进行相关方面计算的内容.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
15.物质的性质决定物质的用途.下列物质的用途中,主要利用其物理性质的是( )
| A. | 天然气用来作燃料 | B. | 二氧化碳用来作灭火 | ||
| C. | 干冰用作制冷剂 | D. | 氮气用作焊接金属的保护气 |
5.学习了“盐”后,小芳知道了亚硝酸钠(NaNO2)有毒但在超市里她发现某品牌熟肉制品的标签上标有亚硝酸钠.这一现象引起了小芳对食品添加剂的关注.査阅了大量资料后她收集到的信息如表:
山梨酸钾(C5H7COOK)为白色固体,由离子构成,水溶液的pH约为8,由于它价格偏高,有些不法商家在其中掺入碳酸钾作假,碳酸钾不具备防腐作用.
必须指出的是一直受到人们谴责的三聚氰胺、苏丹红等并不是食品添加剂.是严禁加入食品的非法添加物,请回答:
(1)食品添加剂NaNO2中氮元素的化合价为+3.
(2)分析以上资料.山梨酸钾中起防腐作用的是山梨酸根离子.而不是钾离子;
(3)为检验某商家在出售的山梨酸押中掺入了碳酸钾,请写出检验的试剂稀盐酸(或CaCl2溶液);
(4)阅读文章后,下列有关食品添加剂的认识正确的是b、c.
a.食品添加剂对人体都有害应该禁止使用
b.山梨酸钾能有效保持食品的新鲜,可以按安全标准量添加
c.某些有毒物质合理使用也能让其发挥作用.
| 添加剂类别 | 主要作用 | 常见的添加剂 | 使用注意事项 |
| 防腐剂 | 抑菌防腐,延长保质期 | 亚硝酸钠、山梨酸钾等 | 绝不能超过安全标准 用量,否则有安全风险 |
| 酸化剂 | 改善食品的口味 | 柠梭酸,乳酸、苯甲酸等 | |
| 膨松剂 | 使食品蓬松 | 碳酸氢钠.碳酸氢铵等 |
必须指出的是一直受到人们谴责的三聚氰胺、苏丹红等并不是食品添加剂.是严禁加入食品的非法添加物,请回答:
(1)食品添加剂NaNO2中氮元素的化合价为+3.
(2)分析以上资料.山梨酸钾中起防腐作用的是山梨酸根离子.而不是钾离子;
(3)为检验某商家在出售的山梨酸押中掺入了碳酸钾,请写出检验的试剂稀盐酸(或CaCl2溶液);
(4)阅读文章后,下列有关食品添加剂的认识正确的是b、c.
a.食品添加剂对人体都有害应该禁止使用
b.山梨酸钾能有效保持食品的新鲜,可以按安全标准量添加
c.某些有毒物质合理使用也能让其发挥作用.
12.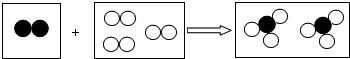 如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )
如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )
 如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )
如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 参加反应的两种物质的分子个数比为2:3 | |
| D. | 共有两种元素参与反应 |
10.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 确定某未知溶液中含有SO42- | 先滴加稀盐酸,无明显现象,再滴加BaCl2溶液,产生白色沉淀 |
| D | 除去CaO中的CaCO3 | 加入水溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
 (1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)
(1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)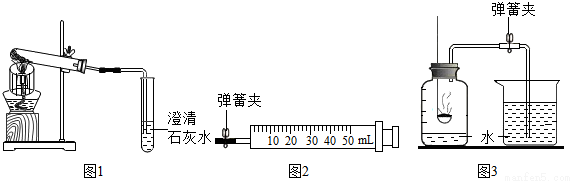
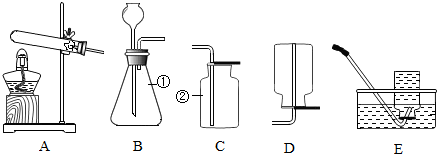
 水是一种重要的自然资源.
水是一种重要的自然资源.