题目内容
15.下列装置常用于实验制取气体.根据给出的装置回答下列问题: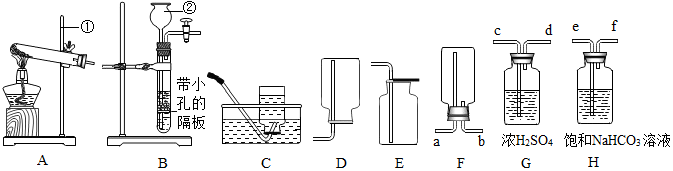
(1)指出编号仪器名称:①铁架台;②长颈漏斗.
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.利用C装置收集氧气的最佳时刻是当导管口有连续均匀气泡冒出时.
(3)制取并收集二氧化碳应选择的装置是BE(从A~E中选择),使用该套装置制取气体的突出优点是可以控制反应的发生和停止,该反应原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.若改用F装置收集二氧化碳,则气体应从b端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使个G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→C.(填序号)
A.c→d→e→fB.d→c→f→eC.e→f→c→dD.f→e→d→c
(4)某同学取3.16g高锰酸钾固体加热一段时间,经检测固体中钾原子与氧原子个数比为2:7,则生成的氧气质量为0.16g.
分析 (1)熟记仪器的名称;
(2)根据实验室制取氧气的原理以及装置选择依据和注意事项来分析;
(3)根据气体发生和收集装置的选择依据、反应的原理以及除杂方法来分析;
(4)根据质量守恒定律,利用反应前后钾元素的质量不变分析解答.
解答 解:(1)铁架台是常用的夹持仪器,长颈漏斗方便加液体药品,故答案为:铁架台;长颈漏斗;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;当导管口有连续均匀气泡冒出时;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;使用B装置制取气体的突出优点是:可以控制反应的发生和停止;故答案为:BE;可以控制反应的发生和停止;
因为二氧化碳的密度比空气大,故应该从短管进入集气瓶的下方,将空气挤压到集气瓶上部排出;制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,应该先通过饱和的碳酸氢钠溶液除去氯化氢气体,再通过浓硫酸吸收水而得到干燥的纯净的二氧化碳,且洗气装置导管长进短出,故连接顺序为:efcd.
故答案为:b;C;
(4)设反应后氧元素的质量为x,
3.16g高锰酸钾中,钾元素的质量为:3.16g×$\frac{39}{158}$=0.78g
氧元素的质量为:3.16g×$\frac{64}{158}$=1.28g
剩余物中钾和氧的原子个数比为2:7时,锰元素和氧元素的质量比为:(39×2):(16×7)=39:56,
反应前后钾元素的质量不变,则有:39:56=0.78g:x,
x=1.12g,
则加热过程中产生氧气的质量为:1.28g-1.12g=0.16g,
故答案为:0.16g.
点评 本题考查了常见气体的制取和收集、除杂,是中考的重点考查方式,关键是明确发生装置、收集方法选择的依据.

| A. | 碳在氧气中燃烧放出白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色的火焰 | |
| C. | 铁丝在氧气中燃烧生成黑色的四氧化三铁 | |
| D. | 一氧化碳在空气中燃烧产生蓝色火焰 |
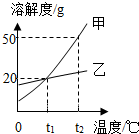 甲、乙两种物质的溶解度曲线如图所示,下列说法错误的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法错误的是( )| A. | t1℃时,甲和乙的溶解度相等 | |
| B. | t1℃时,20g乙加到100g水中形成饱和溶液 | |
| C. | t2℃时,甲乙各100g饱和溶液降温到t1℃析出的晶体甲比乙多30g | |
| D. | 若家中含有少量乙,提纯甲可用冷却热饱和溶液的方法 |
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液;
(2)小亮取少最样品于试管中,滴加无色酚酞试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学设计了下面的实验:
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 实验一:取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸) | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl,(Na2CO3+2HCl═2NaCl+H2O+CO2↑) |
| 实验二:取少量溶液于试管中,滴加硫酸铜溶液 | 产生蓝色沉淀 | 该溶液是氢氧化钠溶液. |
原因是因为碳酸钠与氢氧化铜反应也能生成蓝色沉淀.
| 添加剂类别 | 主要作用 | 常见的添加剂 | 使用注意事项 |
| 防腐剂 | 抑菌防腐,延长保质期 | 亚硝酸钠、山梨酸钾等 | 绝不能超过安全标准 用量,否则有安全风险 |
| 酸化剂 | 改善食品的口味 | 柠梭酸,乳酸、苯甲酸等 | |
| 膨松剂 | 使食品蓬松 | 碳酸氢钠.碳酸氢铵等 |
必须指出的是一直受到人们谴责的三聚氰胺、苏丹红等并不是食品添加剂.是严禁加入食品的非法添加物,请回答:
(1)食品添加剂NaNO2中氮元素的化合价为+3.
(2)分析以上资料.山梨酸钾中起防腐作用的是山梨酸根离子.而不是钾离子;
(3)为检验某商家在出售的山梨酸押中掺入了碳酸钾,请写出检验的试剂稀盐酸(或CaCl2溶液);
(4)阅读文章后,下列有关食品添加剂的认识正确的是b、c.
a.食品添加剂对人体都有害应该禁止使用
b.山梨酸钾能有效保持食品的新鲜,可以按安全标准量添加
c.某些有毒物质合理使用也能让其发挥作用.
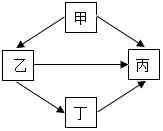 甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题:
甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题: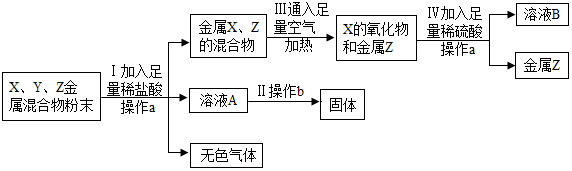
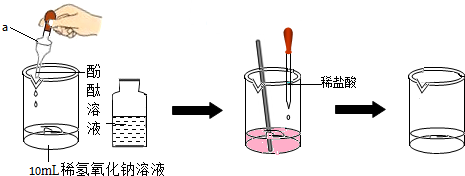
 (1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)
(1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)