题目内容
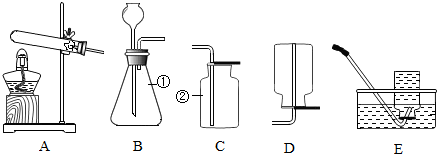
18.一同学用某种粗盐进行提纯实验,步骤见图.
请回答:
(1)步骤①和②的操作名称是过滤.
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡放出为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成固体(或溶液)飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 有气泡放出,石灰水变浑浊 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想II不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量制得的NaCl晶体溶于试管中的蒸馏水,滴入BaCl2 | 有白色沉淀 | 猜想Ⅲ成立 |
分析 (1)根据过滤是将液体和固体进行分离的一种操作进行分析;
(2)根据盐酸会与碳酸钠反应产生二氧化碳,蒸发皿是热的不良导体在加热时会造成液滴飞溅;
(3)根据猜想I、II、III进行对比分析解答,还要结合猜想物质的性质进行分析.
解答 解:(1)经过①的操作分离出了可溶物和不溶物,所以步骤①和②的操作名称是过滤;
(2)因为盐酸和碳酸钠反应生成气体,所以再向溶液中滴加稀盐酸看有无气泡产生即可判断稀盐酸的量;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成液滴飞溅; 当蒸发皿中有较多量固体出现时,应停在加热,用余热使水分蒸干;
(3)猜想Ⅰ:碳酸根离子遇到盐酸会产生二氧化碳气体,该气体能使澄清石灰水变浑浊,故答案为:有气泡放出,石灰水变浑浊
猜想Ⅱ:碳酸钡会溶于硝酸,而硫酸钡不会溶于硝酸,故答案为:滴入稀硝酸,猜想Ⅱ不成立
猜想Ⅲ:要检验硫酸根离子需要滴入硝酸酸化的氯化钡,生成不溶于硝酸的白色沉淀,故答案为:滴入BaCl2溶液和稀HNO3,有白色沉淀且不溶于稀HNO3.
故答案为:(1)过滤;
(2)滴加盐酸至恰好无气泡放出为止,局部过热造成固体(或溶液)飞溅,停止加热(或熄灭酒精灯);
(3)
| 验证的方法 | 现象 | 结论 |
| 有气泡放出,烧杯底变浑浊(合理即可) | ||
| 滴入稀硝酸(或稀盐酸) | 猜想Ⅱ不成立 | |
| 滴入BaCl2[或Ba(OH)2、或Ba(NO)3]溶液 | 有白色沉淀 |
点评 本题主要考查了常见离子的检验方法,以及对粗盐提纯实验的综合考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )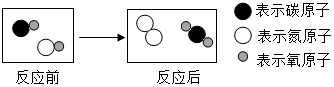

| A. | 图中涉及的物质均为氧化物 | B. | 反应物和生成物均含有毒气体 | ||
| C. | 生成单质与化合物的质量比为7:22 | D. | 生成物的分子个数比为1:1 |
 A到G都是初中化学常见的物质,其中C、D、E、F、G属于不同类别的物质,A、C的组成元素相同,C、F中不含有相同的元素,B为红色粉末.它们之间的相互关系如图所示:(其中“--”表示相连物质间能反应,“→”表示两种物之间的转化关系,部分反应物、生成物及反应条件省略).
A到G都是初中化学常见的物质,其中C、D、E、F、G属于不同类别的物质,A、C的组成元素相同,C、F中不含有相同的元素,B为红色粉末.它们之间的相互关系如图所示:(其中“--”表示相连物质间能反应,“→”表示两种物之间的转化关系,部分反应物、生成物及反应条件省略).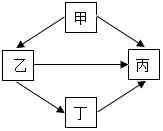 甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题:
甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题:
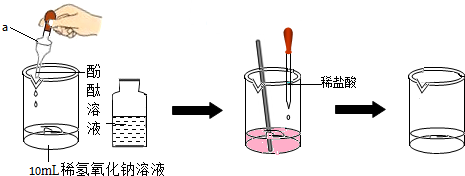
 (1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)
(1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)