题目内容
3.用氢气还原氧化铜的方法测定某氧化铜样品中氧化铜的百分含量(杂质不与氢气反应),同学们设计了以下实验装置,取一定量干燥样品进行实验.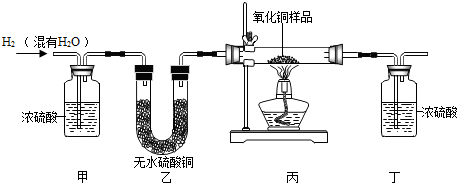
【查阅资料】浓硫酸具有吸水性,可做干燥剂.请根据资料回答:
(1)在实验中,乙装置的作用是检验水是否除尽;丙中的现象是黑色固体变红色.
(2)要得出氧化铜样品的百分含量,需要准确称取的数据是样品质量、反应前后玻璃管及管内固体的质量.
(3)根据以下原因计算,可能导致结果偏大的是B.
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.氧化铜没有完全被还原.
分析 (1)根据无水硫酸铜的性质并结合装置分析其作用,氧化铜和氢气在加热的条件下生成铜和水进行分析;
(2)根据要得出氧化铜样品的百分含量,需要准确称取的数据是样品质量、反应前后玻璃管及管内固体的质量进行分析;
(3)根据实验装置,丁装置与大气相通,空气中含有水蒸气,浓硫酸具有吸水性进行分析解答.
解答 解:(1)无水硫酸铜为白色固体,遇水变成蓝色,故可根据其颜色是否改变判断氢气中水分水分被吸收干净;
氧化铜和氢气在加热的条件下生成铜和水,所以丙中的现象是黑色固体变成红色;
(2)要得出氧化铜样品的百分含量,需要准确称取的数据是样品质量、反应前后玻璃管及管内固体的质量;
(3)根据浓硫酸质量的增加量计算结果偏大,原因是浓硫酸与空气通着,吸收了空气中的水分,故选:B.
故答案为:(1)检验水是否除尽,黑色固体变红色;
(2)样品质量、反应前后玻璃管及管内固体的质量;
(3)B.
点评 本题容易出错的地方是对两种做法不同的原因分析,了解装置的特点及物质的作用是解答的关键,要考虑浓硫酸的吸水性,不仅吸收了生成的水,连空气中的水也吸收了.

练习册系列答案
相关题目
11.下列有关金属及合金的说法中正确的是( )
| A. | 铝、铁、铜都是银白色固体,都能导电 | |
| B. | 铜的化学性质不活泼,所以铜制品不会生锈 | |
| C. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| D. | 硬币、不锈钢锅都是合金材料,合金比各成分金属具有更优良的性能 |
12.下列关于“物质--用途--性质”的说法,其中不正确的是( )
| A. | 稀有气体-霓虹灯-通电能发出不同颜色的光 | |
| B. | 干冰-制冷剂-升华吸热 | |
| C. | 氮气-食品防腐-常温下化学性质稳定 | |
| D. | 石墨-润滑局-质软 |
13.下列物质性质或现象描述错误的是( )
| A. | 合金的硬度比组成它们的纯金属的硬度小 | |
| B. | 消防队员用水降低可燃物的温度来灭火 | |
| C. | 极易与血红蛋白结合的有毒气体是一氧化碳 | |
| D. | 硫在氧气中燃烧产生明亮的蓝紫色火焰 |

