题目内容
18.某气体由 H2、CO 中的一种或两种组成,某化学兴趣小组对该气体的组成进行探究.【提出问题】该气体由什么物质组成?
【提出假设】猜想1:只有氢气;
猜想2:只有一氧化碳;
猜想3:既有氢气又有一氧化碳.
【提供信息】1、由 H2、CO 中的一种或两种组成的气体能在氧气中安静地燃烧.
2、白色的无水CuSO4遇水变蓝色
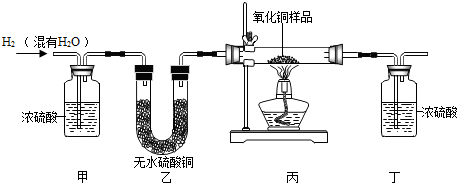
【设计实验】将该气体在氧气中完全燃烧的产物依次通过无水硫酸铜、澄清石灰水,根据两种物质的变化情况来推测该气体的组成.
【现象与结论】①无水硫酸铜变成蓝色,澄清石灰水无明显变化,猜想1成立.
②无水硫酸铜无变化,澄清石灰水变浑浊,猜想2成立.
③无水硫酸铜变成蓝色,澄清石灰水变浑浊,猜想3成立.
【分析讨论】
(1)无水硫酸铜变成蓝色,说明气体燃烧的产物中有水生成,推知该气体成分中一定含有氢元素;澄清石灰水变浑浊,说明该气体燃烧的产物中有二氧化碳生成,推知该气体成分中一定含有碳元素.
(2)写出澄清石灰水变浑浊的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
分析 【提出假设】根据气体X由H2、CO中的一种或两种组成可知有三种可能进行分析;
【现象与结论】根据无水硫酸铜遇水变蓝色,澄清石灰水和二氧化碳会生成碳酸钙沉淀进行分析;
【分析讨论】(1)根据氢元素燃烧生成了水,碳元素燃烧生成了二氧化碳进行分析;
(2)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析.
解答 解:【提出假设】气体X由H2、CO中的一种或两种组成,如果是有一种组成,可以是氢气,可以是一氧化碳,如果是两种就是既有一氧化碳又有氢气;
【现象与结论】①无水硫酸铜变成蓝色,澄清石灰水无明显变化,猜想1成立;
②无水硫酸铜无变化,澄清石灰水变浑浊,猜想2成立;
③无水硫酸铜变成蓝色,澄清石灰水变浑浊,猜想3成立;
【分析讨论】(1)无水硫酸铜变成蓝色,说明气体燃烧的产物中有水生成,推知该气体成分中一定含有氢元素;澄清石灰水变浑浊,说明该气体燃烧的产物中有二氧化碳生成,推知该气体成分中一定含有碳元素;
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:【提出假设】猜想Ⅲ:既有氢气又有一氧化碳;
【现象与结论】①1;
②2;
③3;
【分析讨论】(1)水,氢,二氧化碳,碳;
(2)CO2+Ca(OH)2=CaCO3↓+H2O.
点评 物质的推断是初中化学的难重点,也是中考的热点之一,了解物质的性质是解题的前提条件,解题时还要注意前后步骤间的联系,充分利用综合归纳法得出完整合理的结论.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
10.下列说法正确的是( )
| A. | 由不同种元素组成的物质一定是混合物 | |
| B. | 某物质能与碱反应生成盐和水,则该物质一定是酸 | |
| C. | 向某固体中加入稀盐酸有气体产生,则该固体一定是较活泼金属 | |
| D. | 饱和溶液析出晶体后,溶质质量分数不一定减小 |
9.鉴别空气、氧气和二氧化碳三瓶气体的正确方法是( )
| A. | 闻气体的气味 | B. | 分别插入燃着的木条 | ||
| C. | 观察气体的颜色 | D. | 分别倒入少量的澄清石灰水 |
6.在研究人呼出的气体与空气中二氧化碳有什么不同时,实验小组曾用排水法收集一瓶气体与空气进行对比实验(如图1).对比实验中看到的现象是盛有呼出气体的集气瓶中澄清石灰水变浑浊,而盛有空气的集气瓶中无明显现象,反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.

【提出问题】实验室制取二氧化碳时能不能用排水法收集?
【查阅资料】通常情况下:二氧化碳在饱和碳酸氢钠溶液中
不溶;1体积水约能溶解1体积二氧化碳.
【进行实验】实验小组设计了如图2实验装置进行探究.
(1)A中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)A中充满二氧化碳的目的是避免空气对实验产生干扰.
(3)实验室用排水法收集气体的方法通常如图3所示,则实验小组的研究中,实验装置B还有缺陷,你认为改进的方法是将装置B的左侧导管换成长导管并伸到集气瓶的底部.
(4)改进装置后,再次按照实验1和2的过程进行实验,实验结果为“量筒内液体体积,实验2比实验1少约10%”,说明二氧化碳可以用排水法进行收集.你认为二氧化碳能用排水法收集的原因是二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应.

【提出问题】实验室制取二氧化碳时能不能用排水法收集?
【查阅资料】通常情况下:二氧化碳在饱和碳酸氢钠溶液中
不溶;1体积水约能溶解1体积二氧化碳.
【进行实验】实验小组设计了如图2实验装置进行探究.
| 实验 | 实验过程 | 实验结果 |
| 1 | A中加入足量石灰石,并充满二氧化碳;B中盛满饱和碳酸氢钠溶液.将10mL稀盐酸注入瓶中. | 量筒内液体体积,实验2比实验1少约1%. |
| 2 | A中加入足量石灰石,并充满二氧化碳;B中盛满蒸馏水.将10mL稀盐酸(浓度与实验1相同)注入瓶中. |
(2)A中充满二氧化碳的目的是避免空气对实验产生干扰.
(3)实验室用排水法收集气体的方法通常如图3所示,则实验小组的研究中,实验装置B还有缺陷,你认为改进的方法是将装置B的左侧导管换成长导管并伸到集气瓶的底部.
(4)改进装置后,再次按照实验1和2的过程进行实验,实验结果为“量筒内液体体积,实验2比实验1少约10%”,说明二氧化碳可以用排水法进行收集.你认为二氧化碳能用排水法收集的原因是二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应.
10.下列化学用语中,正确的是( )
| A. | 2个氧分子:2O | B. | 氧化钠:NaO | C. | 一氧化碳:Co | D. | 3个钠离子:3Na+ |