题目内容
8.现代社会对能源的需求量越来越大,能源的开发和利用备受人类关注.(1)化石燃料包括煤、石油和天然气.化石燃料燃烧排放的气体会污染环境,其中含有形成酸雨的主要气体,其化学式为NO2、SO2.
(2)车用乙醇汽油可适当节省石油资源,并在一定程度上减少汽车尾气的污染.乙醇燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
分析 (1)煤、石油和天然气属于化石燃料,是不可再生能源;二氧化硫、氮氧化物是形成酸雨的主要物质.
(2)根据乙醇与氧气在点燃的条件下反应生成水和二氧化碳,写出反应的化学方程式即可;
解答 解:(1)化石燃料包括煤、石油和天然气,它们属于不可再生能源;煤中含有硫,硫燃烧能生成二氧化硫,二氧化硫能和水反应生成亚硫酸,亚硫酸能和氧气反应生成硫酸,氮氧化物能和水反应生成硝酸等物质,当雨水中硫酸、硝酸等物质的含量达到一定程度时,就形成酸雨;
(2)乙醇完全燃烧能生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
故答案为:(1)石油;NO2、SO2;(2)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
点评 本题难度不大,环境污染日趋严重,已经引起人们的高度重视,治理污染初见成效,减少化石燃料的使用,大力开发利用新能源,有利于减缓环境污染;掌握氢气的化学性质、氢能源的优缺点等即可正确解答本题.

练习册系列答案
相关题目
20.某兴趣小组同学对实验室制备氧气的条件进行如下探究.
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是氧化铜.
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热Ⅲ.将3.0g氯酸钾与Xg氧化铜均匀混合加热
【实验现象分析】
Ⅲ中X的值应为1.0,实验Ⅰ和Ⅲ比较可证明氧化铜能加快氯酸钾分解的速率. 现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是比较二氧化锰与氧化铜的催化效果. 将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,然后进行称量的目的是验证氧化铜的质量在化学反应前后是否改变,最后还要再将黑色粉末和氯酸钾混合加热,
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
【实验反思】MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计.)
【讨论交流】图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,产生的氧气越多,反应速率差不多.图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,反应速度越快,产生的氧气一样多.

【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 种类 温度/℃ 反应程度 | 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 |
| 开始反应 | 420℃ | 515℃ | 305℃ | 490℃ |
| 剧烈反应 | 490℃ | 540℃ | 350℃ | 545℃ |
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热Ⅲ.将3.0g氯酸钾与Xg氧化铜均匀混合加热
【实验现象分析】
Ⅲ中X的值应为1.0,实验Ⅰ和Ⅲ比较可证明氧化铜能加快氯酸钾分解的速率. 现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是比较二氧化锰与氧化铜的催化效果. 将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,然后进行称量的目的是验证氧化铜的质量在化学反应前后是否改变,最后还要再将黑色粉末和氯酸钾混合加热,
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
【实验反思】MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计.)
【讨论交流】图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,产生的氧气越多,反应速率差不多.图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,反应速度越快,产生的氧气一样多.

19.近来由于空气质量红色预警,北京市出台了“停课不停学”的方案.复课后同学们带来了空气净化器滤芯上的黑色物质,某实验小组对其成分进行研究.
【查阅资料】
(1)雾霾的成因主要是:工业生产、热电厂排放的水蒸气造成空气湿度增加,在某些气候条件下水蒸气不能及时上升扩散,遇冷凝结形成雾;工业燃煤、燃油、车用燃料不充分燃烧产生的炭粒、碳氢化合物(可燃)以及建筑尘埃等大量混入空气,形成霾.二者结合形成雾霾.
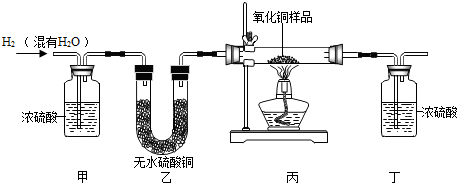
(2)无水硫酸铜为白色固体,遇水变蓝.
【提出问题】黑色物质中是否含有炭粒和水.
【进行实验】

【反思与建议】
(1)组内成员认为结论不严谨,黑色物质中还可能有碳氢化合物,他的理由是碳氢化合物燃烧后也会生成二氧化碳和水.
(2)雾霾的成分非常复杂,通过以上实验只能证明黑色物质中含有碳元素和氢元素,若要了解雾霾的成分,需进一步的学习和研究.
(3)请你对治理雾霾提出合理建议:可使燃料充分燃烧,乘坐公共交通出行.
【查阅资料】
(1)雾霾的成因主要是:工业生产、热电厂排放的水蒸气造成空气湿度增加,在某些气候条件下水蒸气不能及时上升扩散,遇冷凝结形成雾;工业燃煤、燃油、车用燃料不充分燃烧产生的炭粒、碳氢化合物(可燃)以及建筑尘埃等大量混入空气,形成霾.二者结合形成雾霾.
(2)无水硫酸铜为白色固体,遇水变蓝.
【提出问题】黑色物质中是否含有炭粒和水.
【进行实验】

| 实验操作 | 实验现象 | 实验结论 |
| ①向A中通入氧气,排尽空气 | / | / |
| ②连接装置A→C→B | / | / |
| ③点燃酒精灯,充分反应 | 观察到C中白色固体变蓝,B中石灰水变浑浊 | 黑色物质中含有炭粒和水 A中发生反应的化学方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2. |
(1)组内成员认为结论不严谨,黑色物质中还可能有碳氢化合物,他的理由是碳氢化合物燃烧后也会生成二氧化碳和水.
(2)雾霾的成分非常复杂,通过以上实验只能证明黑色物质中含有碳元素和氢元素,若要了解雾霾的成分,需进一步的学习和研究.
(3)请你对治理雾霾提出合理建议:可使燃料充分燃烧,乘坐公共交通出行.
13. 电解熔融Al2O3冶炼铝,化学方程式为2Al2O3$\frac{\underline{\;\;\;\;\;通电\;\;\;\;\;}}{Na_{3}AlF_{6}}$4Al+3O2↑,如图表示一定质量的Al2O3和Na3AlF6固体混合物受热过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
电解熔融Al2O3冶炼铝,化学方程式为2Al2O3$\frac{\underline{\;\;\;\;\;通电\;\;\;\;\;}}{Na_{3}AlF_{6}}$4Al+3O2↑,如图表示一定质量的Al2O3和Na3AlF6固体混合物受热过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
 电解熔融Al2O3冶炼铝,化学方程式为2Al2O3$\frac{\underline{\;\;\;\;\;通电\;\;\;\;\;}}{Na_{3}AlF_{6}}$4Al+3O2↑,如图表示一定质量的Al2O3和Na3AlF6固体混合物受热过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
电解熔融Al2O3冶炼铝,化学方程式为2Al2O3$\frac{\underline{\;\;\;\;\;通电\;\;\;\;\;}}{Na_{3}AlF_{6}}$4Al+3O2↑,如图表示一定质量的Al2O3和Na3AlF6固体混合物受热过程中,某变量y随时间的变化趋势.纵坐标表示的是( )| A. | 生成O2的质量 | B. | 固体中Na3AlF6的质量 | ||
| C. | 固体中氧元素的质量 | D. | 固体中铝元素的质量分数 |
18.如图为某反应的微观示意图,其中不同的球代表不同元素的原子,下列说法错误的是( )


| A. | 反应前后原子的种类和数目都不变 | |
| B. | 生成物可能都是氧化物 | |
| C. | 乙中元素的化合价在反应前后保持不变 | |
| D. | 反应物与生成物的分子个数比为1:1 |
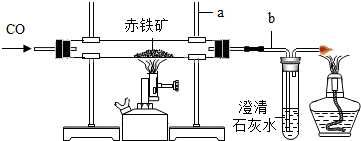 实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).
实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).