题目内容
14.A-H是学过的一些物质,其中A是暗紫色固体,B是人体生命活动离不开的气体,E是淡黄色固体,G是白色固体.它们之间有如图所示的转化关系:
回答下列问题:
(1)写出下列物质的化学式:CMnO2;GKClO3.
(2)反应②的实验:可以观察到的实验现象为:发出蓝紫色的火焰,生成一种有刺激性气味的气体.
(3)写出下列反应的化学方程式:
①2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;②S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
分析 根据A-H是学过的一些物质,B是人体生命活动离不开的气体,所以B是氧气,A是暗紫色固体,A加热会生成氧气,所以A是高锰酸钾,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,G是白色固体,C和G加热也会生成氧气,所以C是二氧化锰,D是锰酸钾,G是氯酸钾,H是氯化钾,E是淡黄色固体,和氧气反应会生成F,所以E是硫,F是二氧化硫,然后将推出的物质进行验证即可.
解答 解:(1)A-H是学过的一些物质,B是人体生命活动离不开的气体,所以B是氧气,A是暗紫色固体,A加热会生成氧气,所以A是高锰酸钾,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,G是白色固体,C和G加热也会生成氧气,所以C是二氧化锰,D是锰酸钾,G是氯酸钾,H是氯化钾,E是淡黄色固体,和氧气反应会生成F,所以E是硫,F是二氧化硫,经过验证,推导正确,所以C是MnO2,G是KClO3;
(2)反应②的实验:可以观察到的实验现象为:发出蓝紫色的火焰,生成一种有刺激性气味的气体;
(3)①高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
②硫和氧气在点燃的条件下生成二氧化硫,化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
故答案为:(1)MnO2,KClO3;
(2)蓝紫色;
(3)①2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
②S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 闻气体的气味 | B. | 分别插入燃着的木条 | ||
| C. | 观察气体的颜色 | D. | 分别倒入少量的澄清石灰水 |
【查阅资料】
(1)雾霾的成因主要是:工业生产、热电厂排放的水蒸气造成空气湿度增加,在某些气候条件下水蒸气不能及时上升扩散,遇冷凝结形成雾;工业燃煤、燃油、车用燃料不充分燃烧产生的炭粒、碳氢化合物(可燃)以及建筑尘埃等大量混入空气,形成霾.二者结合形成雾霾.
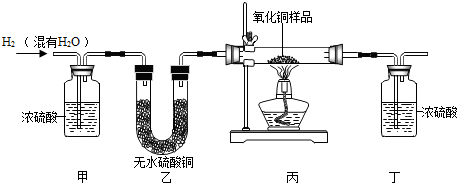
(2)无水硫酸铜为白色固体,遇水变蓝.
【提出问题】黑色物质中是否含有炭粒和水.
【进行实验】

| 实验操作 | 实验现象 | 实验结论 |
| ①向A中通入氧气,排尽空气 | / | / |
| ②连接装置A→C→B | / | / |
| ③点燃酒精灯,充分反应 | 观察到C中白色固体变蓝,B中石灰水变浑浊 | 黑色物质中含有炭粒和水 A中发生反应的化学方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2. |
(1)组内成员认为结论不严谨,黑色物质中还可能有碳氢化合物,他的理由是碳氢化合物燃烧后也会生成二氧化碳和水.
(2)雾霾的成分非常复杂,通过以上实验只能证明黑色物质中含有碳元素和氢元素,若要了解雾霾的成分,需进一步的学习和研究.
(3)请你对治理雾霾提出合理建议:可使燃料充分燃烧,乘坐公共交通出行.

【提出问题】实验室制取二氧化碳时能不能用排水法收集?
【查阅资料】通常情况下:二氧化碳在饱和碳酸氢钠溶液中
不溶;1体积水约能溶解1体积二氧化碳.
【进行实验】实验小组设计了如图2实验装置进行探究.
| 实验 | 实验过程 | 实验结果 |
| 1 | A中加入足量石灰石,并充满二氧化碳;B中盛满饱和碳酸氢钠溶液.将10mL稀盐酸注入瓶中. | 量筒内液体体积,实验2比实验1少约1%. |
| 2 | A中加入足量石灰石,并充满二氧化碳;B中盛满蒸馏水.将10mL稀盐酸(浓度与实验1相同)注入瓶中. |
(2)A中充满二氧化碳的目的是避免空气对实验产生干扰.
(3)实验室用排水法收集气体的方法通常如图3所示,则实验小组的研究中,实验装置B还有缺陷,你认为改进的方法是将装置B的左侧导管换成长导管并伸到集气瓶的底部.
(4)改进装置后,再次按照实验1和2的过程进行实验,实验结果为“量筒内液体体积,实验2比实验1少约10%”,说明二氧化碳可以用排水法进行收集.你认为二氧化碳能用排水法收集的原因是二氧化碳溶解速度慢,二氧化碳不会溶于水或与水反应.

 有A、B、C、D四种物质,其中B是建筑材料的主要成分:C是引起温室效应的主要气体;D与A、B均发生复分解反应.它们之间的相互关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题:
有A、B、C、D四种物质,其中B是建筑材料的主要成分:C是引起温室效应的主要气体;D与A、B均发生复分解反应.它们之间的相互关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题: