题目内容
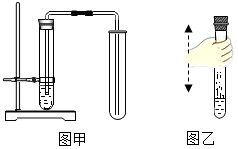
10.实验室中常用分解过氧化氢来简便快速的制备氧气,化学小组进一步探究外界条件对过氧化氢分解速率的影响,并进行了氧气的性质实验.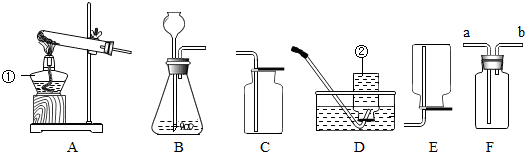
【查阅资料】有些水果、蔬菜对过氧化氢的分解有催化作用.
【实验探究1】探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6mL的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管内,观察现象并记录如下:
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | ||||
取10mL30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100mL氧气所用的时间,(其他实验条件均相同)记录如下:
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | |||
分析 【实验探究】根据苹果、土豆对过氧化氢的分解从反应速率、产生气泡复燃情况进行分析;
【实验探究2】根据表中相同的量和不同的量,结合控制变量法进行分析;
【实验探究3】根据硫和氧气在点燃的条件下生成二氧化硫进行分析.
解答 解:【实验探究】通过分析表中的数据可以看出,苹果和土豆都能催化过氧化氢分解,但是土豆的效果较好,
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | 苹果、土豆对过氧化氢的分解均有催化作用,但催化效果不同或土豆催化效果较好 | |||
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | 浓度越大,反应速率越快 | ||
故答案为:【实验探究1】苹果、土豆对过氧化氢的分解均有催化作用,但催化效果不同或土豆催化效果较好;
【实验探究2】浓度越大,反应速率越快;
【实验探究3】S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
点评 在解此类题时,首先分析题中考查的问题,然后结合题中所给知识和学过的知识,将考查点转化成简单的知识点进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.实验室常用的制取气体的发生装置如图1:
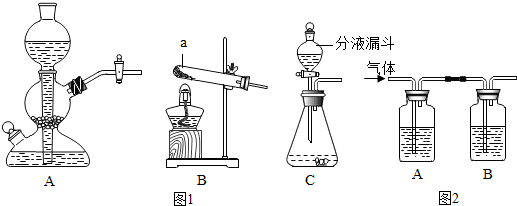
①搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.用此装置作为实验室高锰酸钾制氧气的发生装置,需要进行的改进是在试管口塞一团棉花.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
I.上述实验中反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
II.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
III.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是反应物的接触面积.
IV.实验室制取二氧化碳通常选择稀盐酸而不选择浓盐酸,理由是浓盐酸易挥发,导致二氧化碳中含有氯化氢.
图2的两个洗气瓶中都装有澄清石灰水,将使用浓盐酸制得的二氧化碳从左端通入观察到的现象是A中无明显现象,B中澄清石灰水变浑浊.
Ⅴ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是AB(选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳地产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.

①搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.用此装置作为实验室高锰酸钾制氧气的发生装置,需要进行的改进是在试管口塞一团棉花.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
| 药品 实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | m g,块状 | m g,块状 | m g,粉末状 | m g,粉末状 |
| 盐酸(过量) | w g,稀盐酸 | w g,浓盐酸 | w g,稀盐酸 | w g,浓盐酸 |
II.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
III.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是反应物的接触面积.
IV.实验室制取二氧化碳通常选择稀盐酸而不选择浓盐酸,理由是浓盐酸易挥发,导致二氧化碳中含有氯化氢.
图2的两个洗气瓶中都装有澄清石灰水,将使用浓盐酸制得的二氧化碳从左端通入观察到的现象是A中无明显现象,B中澄清石灰水变浑浊.
Ⅴ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是AB(选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳地产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C |
15.物质的用途主要由物质的性质决定.下列物质的用途是由其化学性质决定的是( )
| A. | 铜丝做导线 | B. | 石墨做铅笔芯 | C. | 铁做锅 | D. | 酒精做燃料 |
19.区分下列各组物质,选择的试剂或方法不正确的是( )
| 物质 | 选用的试剂和方法 | |
| A | 空气、氧气和氮气 | 燃着的木条 |
| B | 硬水和软水 | 肥皂水 |
| C | 盐酸溶液和硫酸溶液 | 碳酸钠溶液 |
| D | 棉纤维和羊毛纤维 | 抽丝灼烧 |
| A. | A | B. | B | C. | C | D. | D |
 已知氢氧化钠固体具有强烈的腐蚀性,王妙雅同学在实验室中需要称量一定量的氢氧化钠固体,量取一定量的水,称量的方法如图所示:
已知氢氧化钠固体具有强烈的腐蚀性,王妙雅同学在实验室中需要称量一定量的氢氧化钠固体,量取一定量的水,称量的方法如图所示: 如图为取用液体药品的示意图,仔细观察,回答下列问题:
如图为取用液体药品的示意图,仔细观察,回答下列问题: