题目内容
2.今年我市初中化学实验考察的内容是“实验室制取二氧化碳气体”,请回答下列相关问题.(1)下列有关连接仪器方法的叙述,错误的是C.
A.将单孔胶塞的约二分之一旋进试管口
B.乳胶管与玻璃导管连接前用水湿润管口
C.乳胶管一端塞进玻璃导管内
D.玻璃导管口一端旋进乳胶管一端
(2)①图甲是某人设计的制备二氧化碳的示意图,其中有2处错误.
②写出实验室制备二氧化碳气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
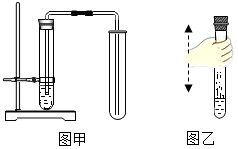
(3)如图乙所示,向集满CO2的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,上、下持续振荡一段时间.
①请写出实验室鉴定CO2的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O;
②充分振荡后,试管内压强<(填“>”“=”或“<”)试管外大气压强;
③振荡试管前,旋紧胶塞的目的是:防止液体流出.
分析 实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
把气体通入澄清石灰水中,如果澄清石灰水变浑浊,说明是二氧化碳.
解答 解:(1)A.将单孔胶塞的约二分之一旋进试管口,该方法正确;
B.乳胶管与玻璃导管连接前用水湿润管口,该方法正确;
C.乳胶管一端塞进玻璃导管内,该方法不正确;
D.玻璃导管口一端旋进乳胶管一端,该方法正确.
故填:C.
(2)①图甲中错误之处:铁夹夹的试管位置偏下;导管口伸入液体中,因此有2处错误;
②实验室制备二氧化碳气体的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:2;CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)①实验室鉴定二氧化碳应该用澄清石灰水,二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
②充分振荡后,由于二氧化碳和氢氧化钙反应,因此试管内压强<试管外大气压强;
③振荡试管前,旋紧胶塞的目的是防止液体流出,从而防止发生事故和导致实验失败.
故填:Ca(OH)2+CO2═CaCO3↓+H2O;<;防止液体流出.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案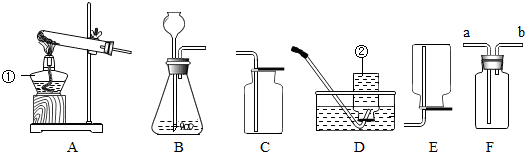
【查阅资料】有些水果、蔬菜对过氧化氢的分解有催化作用.
【实验探究1】探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6mL的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管内,观察现象并记录如下:
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | ||||
取10mL30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100mL氧气所用的时间,(其他实验条件均相同)记录如下:
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | |||
| A. | 化学变化和化学反应是同一个概念 | |
| B. | 物质发生化学变化时一定同时发生物理变化 | |
| C. | 化学变化的特征就是有新物质生成 | |
| D. | 有发光放热等现象的变化一定是化学变化 |
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠(Na2CO3 ) 猜想b:碳酸氢钠(NaHCO3)
小周同学认为猜想b不成立,理由是反应物中没有氢(H) 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸(稀HCl),产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验操作 | 实验现象 | 结论 |
| 1、取适量过氧化钠放入盛有水的烧杯中 | 固体溶解得无色溶液有能使带火星的木条复燃的气体生成. | 有氧气生成 |
| 2、向所得溶液中滴入硫酸铜溶液 | 有蓝色沉淀生成 | 过氧化钠能(填能否)与水反应 |
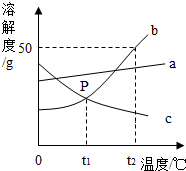 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题: ”表示碳原子,用“
”表示碳原子,用“ ”表示氧原子,用“
”表示氧原子,用“ ”表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题:
”表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题:
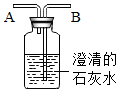 为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验:
为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验: 陈纬同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,用如图所示的装置进行过滤,请问
陈纬同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,用如图所示的装置进行过滤,请问