题目内容
15.现以Mg、C、P、O2、Fe、KMnO4等物质为反应物,按下列要求写出相应的化学方程式:(1)燃烧只生成能使澄清石灰水变浑浊的气体C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)两种非金属单质反应,生成固态物质4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)剧烈燃烧,火星四射,有黑色固体产生3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(4)分解反应,生成物中既有单质又有化合物2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(5)剧烈燃烧,发出耀眼的白光,生成白色的固体2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
分析 (1)根据碳和氧气在点燃的条件下生成二氧化碳进行分析;
(2)根据磷和氧气在点燃的条件下生成五氧化二磷进行分析;
(3)根据铁和氧气在点燃的条件下生成四氧化三铁进行分析;
(4)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(5)根据镁和氧气在点燃的条件下生成氧化镁进行分析.
解答 解:(1)碳和氧气在点燃的条件下生成二氧化碳,化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)磷和氧气在点燃的条件下生成五氧化二磷,化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)铁和氧气在点燃的条件下生成四氧化三铁,化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)镁和氧气在点燃的条件下生成氧化镁,化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
故答案为:(1)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

 阅读快车系列答案
阅读快车系列答案| A. | 给烧杯中液体加热时,在烧杯下面垫上石棉网 | |
| B. | 被加热的玻璃容器外壁如有水,加热前应擦干 | |
| C. | 熄灭酒精灯只能用灯帽盖灭,不能用嘴吹、手扇等方法熄灭 | |
| D. | 用托盘天平称量物质时,先加小砝码再依次加较大的砝码 |
【查阅资料】有些水果、蔬菜对过氧化氢的分解有催化作用.
【实验探究1】探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6mL的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管内,观察现象并记录如下:
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | ||||
取10mL30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100mL氧气所用的时间,(其他实验条件均相同)记录如下:
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | |||
| A. | 化学变化和化学反应是同一个概念 | |
| B. | 物质发生化学变化时一定同时发生物理变化 | |
| C. | 化学变化的特征就是有新物质生成 | |
| D. | 有发光放热等现象的变化一定是化学变化 |
| A. | 为了节约药品,将用剩的药品放回原试剂瓶 | |
| B. | 酒精灯打翻着火,用湿抹布扑盖 | |
| C. | 玻璃仪器用水冲洗三遍就可以 | |
| D. | 药品直接放在天平托盘上称重 |
 取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.
取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.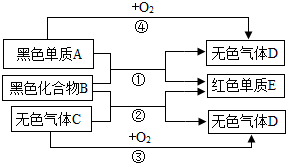 A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去).请回答下列问题:
A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去).请回答下列问题: