题目内容
19.区分下列各组物质,选择的试剂或方法不正确的是( )| 物质 | 选用的试剂和方法 | |
| A | 空气、氧气和氮气 | 燃着的木条 |
| B | 硬水和软水 | 肥皂水 |
| C | 盐酸溶液和硫酸溶液 | 碳酸钠溶液 |
| D | 棉纤维和羊毛纤维 | 抽丝灼烧 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据物质的性质差异进行鉴别,氧气能使燃着的木条燃烧更旺,氮气能灭火,硬水与肥皂水混合产生浮渣,软水与肥皂水混合产生泡沫,盐酸、硫酸都会与碳酸钠反应生二氧化碳气体,羊毛纤维燃烧有烧焦羽毛的气味进行分析.
解答 解:A、燃着的木条在空气中燃烧现象不变,氧气能使燃着的木条燃烧更旺,氮气能灭火,现象不同,可以区分,故A正确;
B、硬水与肥皂水混合产生浮渣,软水与肥皂水混合产生泡沫,现象不同,可以区分,故B正确;
C、盐酸、硫酸都会与碳酸钠反应生二氧化碳气体,不能鉴别,故C错误;
D、羊毛纤维燃烧有烧焦羽毛的气味,而棉纤维燃烧无烧焦羽毛的气味,现象不同,可以区分,故D正确.
故选:C.
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.

练习册系列答案
相关题目
3.下列现象描述不正确的是( )
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 铁丝加入硫酸铜溶液有红色固体生成 | |
| C. | 电解水时正、负两极生成气体体积之比为2:1 | |
| D. | 木炭在氧气中燃烧发出白光 |
10.实验室中常用分解过氧化氢来简便快速的制备氧气,化学小组进一步探究外界条件对过氧化氢分解速率的影响,并进行了氧气的性质实验.
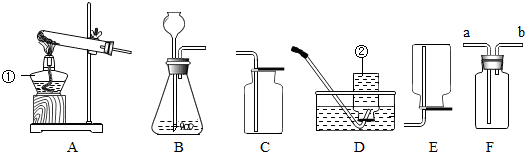
【查阅资料】有些水果、蔬菜对过氧化氢的分解有催化作用.
【实验探究1】探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6mL的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管内,观察现象并记录如下:
【实验探究2】探究浓度对过氧化氢分解速率的影响:
取10mL30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100mL氧气所用的时间,(其他实验条件均相同)记录如下:
【实验条件3】用上述收集的氧气与不同物质进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,该反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.

【查阅资料】有些水果、蔬菜对过氧化氢的分解有催化作用.
【实验探究1】探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6mL的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管内,观察现象并记录如下:
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | ||||
取10mL30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100mL氧气所用的时间,(其他实验条件均相同)记录如下:
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | |||
7.下列说法你认为错误的是( )
| A. | 化学变化和化学反应是同一个概念 | |
| B. | 物质发生化学变化时一定同时发生物理变化 | |
| C. | 化学变化的特征就是有新物质生成 | |
| D. | 有发光放热等现象的变化一定是化学变化 |
4.下列实验基本操作或事故处理,正确的是( )
| A. | 为了节约药品,将用剩的药品放回原试剂瓶 | |
| B. | 酒精灯打翻着火,用湿抹布扑盖 | |
| C. | 玻璃仪器用水冲洗三遍就可以 | |
| D. | 药品直接放在天平托盘上称重 |
11.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠(Na2CO3 ) 猜想b:碳酸氢钠(NaHCO3)
小周同学认为猜想b不成立,理由是反应物中没有氢(H) 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸(稀HCl),产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
解释与结论:写出过氧化钠与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠(Na2CO3 ) 猜想b:碳酸氢钠(NaHCO3)
小周同学认为猜想b不成立,理由是反应物中没有氢(H) 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸(稀HCl),产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验操作 | 实验现象 | 结论 |
| 1、取适量过氧化钠放入盛有水的烧杯中 | 固体溶解得无色溶液有能使带火星的木条复燃的气体生成. | 有氧气生成 |
| 2、向所得溶液中滴入硫酸铜溶液 | 有蓝色沉淀生成 | 过氧化钠能(填能否)与水反应 |
9.质量分数为5%的医用双氧水在常温下难分解;但在双氧水溶液中加入铁锈,就会迅速分解.
【提出问题】铁锈能否起到类似MnO2的催化剂作用呢?
【猜想】Ⅰ:铁锈不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ:铁锈参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ:铁锈是该反应的催化剂,反应前后质量和化学性质不变.

【实验】用天平称量0.2g铁锈,取5mL5%的双氧水于试管中,进行如下实验:
填写下表:
步骤①的目的是与②③进行对比
步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
【拓展】通过步骤⑤得到的固体与原固体相比,你能得出哪些结论催化剂在反应前后质量和化学性质不变.
【提出问题】铁锈能否起到类似MnO2的催化剂作用呢?
【猜想】Ⅰ:铁锈不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ:铁锈参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ:铁锈是该反应的催化剂,反应前后质量和化学性质不变.

【实验】用天平称量0.2g铁锈,取5mL5%的双氧水于试管中,进行如下实验:
填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 带火星的木条复燃 | 铁锈的质量仍为0.2g | 铁锈的质量仍为0.2g | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
【拓展】通过步骤⑤得到的固体与原固体相比,你能得出哪些结论催化剂在反应前后质量和化学性质不变.
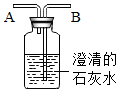 为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验:
为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验: ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)
”表示氢原子)