|
物理量 |
质量分数 |
物质的量浓度 |
溶解度 |
|
溶质单位 |
|
|
|
|
溶液单位 |
|
|
|
|
单
位 |
|
|
|
|
数值上关系 |
质量分数相同的两溶液其物质的量浓度一般 等. |
物质的量浓度相同的两溶液其质量分数一般 等. |
溶质溶解度相同的两溶液其在同一温度下饱和溶液的质量分数 等. |
|
定 义 |
|
|
|
|
符号 |
|
|
|
|
表达式 |
|
|
|
|
相同点 |
都能示溶质和溶液的相对比值 |
||
|
转化关系 |
|
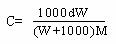
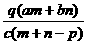 B
B 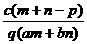 C
C 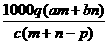 D
D 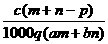
 %、ρ之间的计算关系
%、ρ之间的计算关系 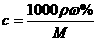
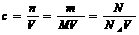
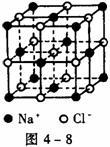
 g/cm3,晶胞边长为4.28×10-10m。
g/cm3,晶胞边长为4.28×10-10m。